
题目列表(包括答案和解析)
 )泄漏致使多人受伤事件。芥子气被称为“毒气之王”,它为无色油状液体,工业品呈棕褐色,有大蒜气味,沸点
)泄漏致使多人受伤事件。芥子气被称为“毒气之王”,它为无色油状液体,工业品呈棕褐色,有大蒜气味,沸点A.它能与漂白粉反应 B.它能发生水解反应
C.它易溶于水和汽油 D.它能发生消去反应
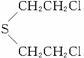
(1)经过分析,芥子气的分子中与—S—相连的两个完全相同、不含甲基的原子团,则芥子气分子的结构简式为__________。
(2)芥子气常用如图1-4-8两种方法合成
Ⅰ.
图1-4-8
Ⅱ.2B+S2Cl2![]() C4H8SCl2(芥子气)+D(已经配平)
C4H8SCl2(芥子气)+D(已经配平)
①写出反应a的化学方程式:________________,反应b的化学方程式:__________________,反应b属于_______反应(填反应类型);每生成1摩尔芥子气,需要消耗______摩尔HCl。
②D属于________晶体,若试管内壁粘有固体D,可用________洗涤除去。已知S2Cl2分子中所有的原子都满足8个电子的稳定结构,其电子式为________。
③芥子气能与氢氧化钠溶液发生类似卤代烃水解的反应,写出它们与氢氧化钠反应的方程式:____________________________________________________________________。
④对于局部芥子气中毒时,可以采取________ (填序号)措施进行简单的处理。
A.用酒精擦试去毒液
B.用漂白粉、双氧水的稀溶液浸润的棉球擦试减缓它的毒性
C.用氢氧化钠的浓溶液洗涤

 这样便得到了高纯度的纳米铁粉.
这样便得到了高纯度的纳米铁粉.
| ||
| ||
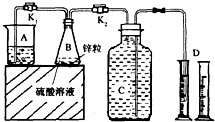 某化学兴趣小组用如图装置进行“市售锌粒和硫酸反应制取氢气的条件选择”的探究:当B中的化学反应趋于平稳后,每间隔一分钟收集一次氢气.不同条件下,每分钟收集到氢气的体积如下表:
某化学兴趣小组用如图装置进行“市售锌粒和硫酸反应制取氢气的条件选择”的探究:当B中的化学反应趋于平稳后,每间隔一分钟收集一次氢气.不同条件下,每分钟收集到氢气的体积如下表:| 实验序号 | 硫酸浓度 | 饱和硫酸铜溶液体积/mL | 反应达到平稳的时间/min | 第1分钟收集氢气体积/mL | 第2分钟收集氢气体积/mL | 第3分钟收集氢气体积/mL | … |
| 1 | 20% | 0 | 5.4 | 6.1 | 11.9 | 13.7 | … |
| 2 | 20% | 0.5 | 2.5 | 23.9 | 32.1 | 33.5 | … |
| 3 | 30% | 0.5 | 1.1 | 60.7 | 89.9 | 90.1 | … |
| 4 | a% | 3.0 | 0.8 | 55.7 | 66.0 | 61.4 | … |
| 2 |
| 5 |
| ||

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com