
题目列表(包括答案和解析)
(09全国卷2,27)某温度时,在2L密闭容器中气态物质X和Y反应生成气态物质Z,它们的物质的量随时间的变化如表所示。
(1)根据表中数据,在图中画出X、Y、Z的物质的量(n)随时间(t)变化的曲线:
t/min | X/mol | Y/mol | Z/mol |
0 | 1.00 | 1.00 | 0.00 |
1 | 0.90 | 0.80 | 0.20 |
3 | 0.75 | 0.50 | 0.50 |
5 | 0.65 | 0.30 | 0.70 |
9 | 0.55 | 0.10 | 0.90 |
10 | 0.55 | 0.10 | 0.90 |
14 | 0.55 | 0.10 | 0.90 |

(2) 体系中发生反应的化学方程式是___________________________;
(3) 列式计算该反应在0-3min时间内产物Z的平均反应速率:_______________;
(4) 该反应达到平衡时反应物X的转化率![]() 等于___________________________;
等于___________________________;
(5) 如果该反应是放热反应。改变实验条件(温度、压强、催化剂)得到Z随时间变化的曲线①、②、③(如右图所示)则曲线①、②、③所对应的实验条件改变分别是:
① _________________ ②________________ ③__________________
(09盐城第三次调研)用NA表示阿伏加德罗常数的值。下列叙述正确的是
A.常温常压下22.4L的CO2在一定条件下与足量的镁反应,转移 4NA个电子
4NA个电子
B.23g钠与一定量的氧气作用,若两者均无剩余,转移NA个电子
C.1mol/L(NH4)2SO4溶液中,含SO42-NA个,NH4+少于2NA个
D.0.5mol雄黄(As4S4,结构如右图)含有NA个S―S键
(09盐城第三次调研)氨催化氧化是硝酸工业的基础,在某催化剂作用下只发生主反应①和副反应②
![]() 4NH3(g) +5O2
4NH3(g) +5O2![]() 4NO(g)+6H2O(g);△H=-905kJ/mol………………①
4NO(g)+6H2O(g);△H=-905kJ/mol………………①
![]() 4NH3(g) + 3O2(g)
4NH3(g) + 3O2(g) ![]() 2N2(g) + 6H2O(g);△H=-1268kJ/mol………②;
2N2(g) + 6H2O(g);△H=-1268kJ/mol………②;
![]()
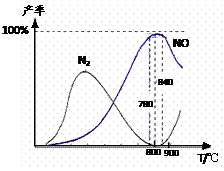 下列说法正确的是
下列说法正确的是
![]() A.工业上进行氨催化氧化生成 NO时,温度应控制在780~840℃之间
A.工业上进行氨催化氧化生成 NO时,温度应控制在780~840℃之间
![]() B.工业上采用物料比n(O2)/n(NH3)在1.7~2.0,主要是为了提高反应速率
B.工业上采用物料比n(O2)/n(NH3)在1.7~2.0,主要是为了提高反应速率
![]() C.在加压条件下生产能力可提高5~6倍,是因为加压可提高转化率
C.在加压条件下生产能力可提高5~6倍,是因为加压可提高转化率
D.氮气氧化为NO的热化学方程式为:N2(g)+ O2(g) ![]() 2NO(g);
2NO(g);
△H=+181.5 kJ/mol
 (09上海奉贤区4月模拟) 分析右边的能量变化示意图,下列热化学方程式中,正确是
(09上海奉贤区4月模拟) 分析右边的能量变化示意图,下列热化学方程式中,正确是
A. 2A(g)+B(g) → 2C(g)+ Q (Q>0)
B. 2A(g)+B(g) → 2C(g)+ Q (Q<0)
C. 2A + B → 2C + Q (Q>0)
D. 2C → 2A + B + Q (Q<0)
(09上海奉贤区4月模拟) 设NA代表阿伏加德罗常数,下列说法正确的是
A.1.8g重水(D2O)中含NA个中子
B.在铜与硫的反应中,1 mol铜失去的电子数为2NA
C.在25℃时,压强为1.01×105帕时,11.2L氧气所含的原子数为NA
D.0.5mol铝与足量烧碱溶液反应,转移的电子数为1.5NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com