
题目列表(包括答案和解析)
(9分)有下列化学仪器:①托盘天平;②玻璃棒;③药匙;④烧杯;⑤量筒;⑥容量瓶;⑦胶头滴管;⑧细口试剂瓶;⑨标签纸。
(1) 现需要配制500 mL 1 mol/L硫酸溶液,需用质量 分数为98%、密度为1.84g/㎝3的浓硫酸______ mL。(小数点后保留1位有效数字)
分数为98%、密度为1.84g/㎝3的浓硫酸______ mL。(小数点后保留1位有效数字)
(2) 从上述仪器中,按实验使用的先后顺序,其编号排列是________
(3) 容量瓶使用前检验漏水的方法是____________
(4)若实验遇到下列情况,对所配制硫酸溶液的物质的量浓度有何影响(填“偏高”、“偏低”或“不变”)?
①用以稀释硫酸的烧杯未洗涤__________
②未经冷却趋热将溶液注入容量瓶中___________
③摇匀后发现液面低于刻度线再加水_____________
④容量瓶中原有少量蒸馏水_____________
⑤定容时俯视观察液面__________________
(9分)电解原理在化学工业中有广泛应用。右图表示一个电解池,其中a为电解质溶液, X、Y是两块电极板,通过导线与直流电源相连。请回答以下问题:
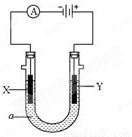
(1)X的电极名称是 (填写“阳极”或“阴极”)。
(2)若要用该装置电解精炼粗铜,电解液a选用CuSO4溶液,则X电极的材料是 ,Y电极的材料是 。
(3)若X、Y都是惰性电极,a是饱和食盐水,实验开始时,同时在两边各滴入几滴酚酞试液,一段时间后,在X极附近观察到的现象是 ,Y极上的电极反应式为 。
(4)若要用电镀方法在铁表面镀一层金属银,应该选择的方案是 。
|
方案 |
X |
Y |
a溶液 |
|
A |
银 |
石墨 |
AgNO3 |
|
B |
银 |
铁 |
AgNO3 |
|
C |
铁 |
银 |
Fe(NO3)3 |
|
D |
铁 |
银 |
AgNO3 |
(10分)
现用质量分数为36.5%、密度为1.20 g·cm-3的浓盐酸来配制100 mL 1.5 mol/L的稀盐酸。可供选择的仪器有:①玻璃棒②烧瓶③烧杯④胶头滴管⑤量筒⑥容量瓶⑦托盘天平⑧药匙。请回答下列问题:
(1)上述仪器中,在配制稀盐酸时用不到的有 (填代号)。
(2)经计算,需浓盐酸的体积为 。
现有①10 mL ②20 mL ③50 mL ④100 mL四种规格的量筒,取用浓盐酸应选用的量筒是 (填代号)。
(3)在配制过程中,其他操作都准确,下列操作中:错误的是 ,能引起误差偏高的有 (填序号)。
①洗涤量取浓盐酸后的量筒,并将洗涤液转移到容量瓶中
②稀释后的盐酸在空气中放置过久
③定容时,加蒸馏水超过标线,又用胶头滴管吸出
④转移前,容量瓶中含有少量蒸馏水
⑤定容摇匀后,发现液面低于标线,又用胶头滴管加蒸馏水至标线
⑥定容时,俯视标线
(9分)已知:① A是石油裂解气的主要成份,A的产量通常用来衡量一个国家的石油化工水平 ② 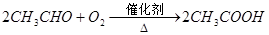 。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
。现以A为主要原料合成乙酸乙酯,其合成路线如下图所示。
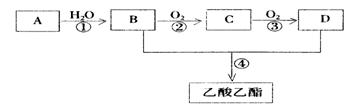
回答下列问题:
(1)B、D分子中的官能团名称分别是 、 。
(2)写出下列反应的反应类型:① ,② ,④ 。
(3)写出下列反应的化学方程式:
② ;④ 。
(9分)酸碱中和滴定是中学化学常见实验。
某同学欲测定某浓硫酸样品的物质的量浓度,进行了以下实验操作:
A.冷却至室温后,在100mL容量瓶中定容配成100mL稀硫酸。
B.量取20.00mL稀硫酸于锥形瓶中并滴入几滴指示剂。
C.将酸式滴定管和碱式滴定管用蒸馏水洗涤干净,并用各待盛溶液润洗。
D.将物质的量浓度为1.50mol/L标准NaOH溶液装入碱式滴定管,调节液面记下读数V1。
E.继续滴定至终点,记下读数为V2。
F.在锥形瓶下垫一张白纸,把锥形瓶移到碱式滴定管下小心滴入NaOH标准溶液,边滴边摇动锥形瓶。
G.量取浓硫酸样品5mL,在烧杯中用蒸馏水稀释。
H.重复以上实验。
请回答下列问题:
(1)该实验正确操作步骤的顺序为 → A→ → →D→ → → H
(用编号字母填写)。
(2)量取5mL浓硫酸的仪器是 ;量取20.00mL稀硫酸的仪器是 。
(3)选用的指示剂是 。滴定过程中,视线应注视 ;判断到达滴定终点的现象是 。
(4)下表是实验测得的有关数据:
|
滴定序号 |
待测稀硫酸的体积(mL) |
所消耗NaOH标准溶液液的体积(mL) |
|
|
V1 |
V2 |
||
|
① |
20.00 |
0.50 |
22.60 |
|
② |
20.00 |
6.00 |
27.90 |
请计算出该浓硫酸样品的浓度为 mol·L-1(不必写出计算过程)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com