
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
ИјГә·ПЖшЎўЖыіөОІЖшЦРөДөӘСх»ҜОпЈЁNOxЈ©ЎўТ»Сх»ҜМјөИУРәҰЖшМеЈ¬іЈУГПВБР·Ҫ·ЁҙҰАнЈ¬ТФјхЙЩ¶Ф»·ҫіөДОЫИҫЎЈ
ЈЁ1Ј©¶ФИјГә·ПЖшҪшРРНСПхҙҰАнКұЈ¬іЈАыУГјЧНйҙЯ»Ҝ»№ФӯөӘСх»ҜОпЈ¬ИзЈә
CH4(g)Ј«4NO2(g)ЈҪ4NO(g)Ј«CO2(g)Ј«2H2O(g) ЎчH ЈҪ-574 kJЎӨmol-1
CH4(g)Ј«4NO(g)ЈҪ2N2(g)Ј«CO2(g)Ј«2H2O(g) ЎчH ЈҪ-1160 kJЎӨmol-1
Фт1molCH4Ҫ«NO2»№ФӯОӘN2өД·ҙУҰИИОӘ Ј»
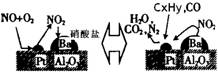
ЈЁ2Ј©іэөӘСх»ҜОпј°COНвЈ¬ЖыіөОІЖшЦР»№ә¬УРМјЗв»ҜәПОпөИОЫИҫОпЈ¬ПВНјКЗЖыіөОІЖшЧӘ»ҜСРҫҝөДКҫТвНјЈәұнКҫөДКЗPt/Al2O3/BaұнГжОьёҪУлҪвОьЧчУГөД»ъАнЈ¬өӘСх»ҜОпКЗNO2Ј¬МјЗв»ҜәПОпКЗCxHyЈ¬РҙіцБҪХЯ·ҙУҰөД»ҜС§·ҪіМКҪЈә Ј¬Pt/Al2O3/BaөДЧчУГКЗ Ј»
ЈЁ3Ј©ЖҪәвіЈКэKөДКэЦөҙуРЎЈ¬КЗәвБҝ»ҜС§·ҙУҰҪшРРіМ¶ИөДұкЦҫЈ¬KөДКэЦөФҪҙ󣬻ҜС§·ҙУҰөДПЮ¶ИФҪҙуЈ¬·ҙУҰОп·ҙУҰөДФҪід·ЦЎЈФЪ25ЎжКұЈ¬ПВБР·ҙУҰөДЖҪәвіЈКэИзПВЈә
N2(g)Ј«O2(g) 2NO(g) K1ЈҪ1ЎБ10Јӯ30 ўе
2H2(g)Ј«O2(g) 2H2O(g) K2ЈҪ2ЎБ1081 ўж
2CO2 (g) 2CO(g)Ј«O2(g) K3ЈҪ4ЎБ10Јӯ92 ўз
![]() ўЩіЈОВПВЈ¬·ҙУҰ2H2O(g) 2H2(g) +O2(g) ЖҪәвіЈКэKЈҪ Ј»
ўЩіЈОВПВЈ¬·ҙУҰ2H2O(g) 2H2(g) +O2(g) ЖҪәвіЈКэKЈҪ Ј»
ўЪ№ШУЪТФЙП·ҙУҰЈ¬ПВБРЛө·ЁХэИ·өДКЗ
AЈ®іЈОВПВЈ¬NOЈ¬H2OЈ¬CO2ИэЦЦ»ҜәПОп·ЦҪв·ЕіцСхЖшөДЗгПтҙуРЎЛіРтЈәNOЈҫH2OЈҫCO2
BЈ®ИфЙэёЯОВ¶ИЈ¬·ҙУҰўзөДЖҪәвіЈКэK3Ҫ«Фцҙу
CЈ®ИфЦ»ФцјУС№ЗҝЈ¬ЗТ·ҙУҰОпЎўЙъіЙОпЧҙМ¬І»ұдЈ¬·ҙУҰўеЖҪәвІ»·ўЙъТЖ¶ҜЈ¬ЖҪәвіЈКэІ»ұдЈ»·ҙУҰўжЖҪәвіҜХэПтТЖ¶ҜЈ¬ЖҪәвіЈКэФцҙу
DЈ®ИфФцјУЖыіө·ў¶Ҝ»ъҝХЖшөДҪшЖшБҝЈ¬ҝЙН¬КұјхЙЩөӘСх»ҜОпәНТ»Сх»ҜМјөДЕЕ·Е
ўЫ»щУЪ»·ұЈ·Ё№жЈ¬ТӘЗуёДЧ°ЖыіөОІЖшҙҰАнЧ°ЦГЈ¬ҙпөҪК№өӘСх»ҜОпЈЁNOЈ©ЎўТ»Сх»ҜМјЧӘ»ҜОӘОЮОЫИҫЎўҝЙЕЕ·ЕөДЖшМеөДДҝөДЎЈёДЧ°өД·Ҫ·ЁЦчТӘКЗјУИлУРР§ҙЯ»ҜјБЈ¬ЗлДгёщҫЭТФЙПУР№ШКэҫЭ·ЦОцЈ¬ФЪІ»ёДұдЖдЛьМхјюөДЗйҝцПВЈ¬ҝЙК№УГҙЯ»ҜјБіэОЫИҫЖшМеөДФӯТтЈә ЎЈ
ИјГә·ПЖшЎўЖыіөОІЖшЦРөДөӘСх»ҜОпЈЁNOxЈ©ЎўТ»Сх»ҜМјөИУРәҰЖшМеЈ¬іЈУГПВБР·Ҫ·ЁҙҰАнЈ¬ТФјхЙЩ¶Ф»·ҫіөДОЫИҫЎЈ
ЈЁ1Ј©¶ФИјГә·ПЖшҪшРРНСПхҙҰАнКұЈ¬іЈАыУГјЧНйҙЯ»Ҝ»№ФӯөӘСх»ҜОпЈ¬ИзЈә
CH4(g)Ј«4NO2(g)ЈҪ4NO(g)Ј«CO2(g)Ј«2H2O(g) ЎчHЈҪ-574 kJЎӨmol-1
CH4(g)Ј«4NO(g)ЈҪ2N2(g)Ј«CO2(g)Ј«2H2O(g) ЎчHЈҪ-1160 kJЎӨmol-1
Фт1molCH4Ҫ«NO2»№ФӯОӘN2өД·ҙУҰИИОӘ Ј»
ЈЁ2Ј©іэөӘСх»ҜОпј°COНвЈ¬ЖыіөОІЖшЦР »№ә¬УРМјЗв»ҜәПОпөИОЫИҫОпЈ¬ПВНјКЗЖыіөОІЖшЧӘ»ҜСРҫҝөДКҫТвНјЈәұнКҫөДКЗPt/Al2O3/BaұнГжОьёҪУлҪвОьЧчУГөД»ъАнЈ¬өӘСх
»№ә¬УРМјЗв»ҜәПОпөИОЫИҫОпЈ¬ПВНјКЗЖыіөОІЖшЧӘ»ҜСРҫҝөДКҫТвНјЈәұнКҫөДКЗPt/Al2O3/BaұнГжОьёҪУлҪвОьЧчУГөД»ъАнЈ¬өӘСх »ҜОпКЗNO2Ј¬МјЗв»ҜәПОпКЗCxHy
»ҜОпКЗNO2Ј¬МјЗв»ҜәПОпКЗCxHy Ј¬РҙіцБҪХЯ·ҙУҰөД»ҜС§·ҪіМКҪЈә Ј¬Pt/Al2O3/BaөДЧчУГКЗ Ј»
Ј¬РҙіцБҪХЯ·ҙУҰөД»ҜС§·ҪіМКҪЈә Ј¬Pt/Al2O3/BaөДЧчУГКЗ Ј»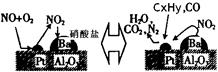
ЈЁ3Ј©ЖҪәвіЈКэKөДКэЦөҙуРЎЈ¬КЗәвБҝ»ҜС§·ҙУҰҪшРРіМ¶ИөДұкЦҫЈ¬KөДКэЦөФҪҙ󣬻ҜС§·ҙУҰөДПЮ¶ИФҪҙуЈ¬·ҙУҰОп·ҙУҰөДФҪід·ЦЎЈФЪ25ЎжКұЈ¬ПВБР·ҙУҰөДЖҪәвіЈКэИзПВЈә
N2(g)Ј«O2(g)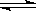 2NO(g) K1ЈҪ1ЎБ10Јӯ30 ўе
2NO(g) K1ЈҪ1ЎБ10Јӯ30 ўе
2H2(g)Ј«O2(g)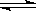 2H2O(g) K2ЈҪ2ЎБ1081 ўж
2H2O(g) K2ЈҪ2ЎБ1081 ўж
2CO2 (g)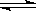 2CO(g)Ј«O2(g) K3ЈҪ4ЎБ10Јӯ92 ўз
2CO(g)Ј«O2(g) K3ЈҪ4ЎБ10Јӯ92 ўз ўЩіЈОВПВЈ¬·ҙУҰ2H2O(g) 2H2(g)
ўЩіЈОВПВЈ¬·ҙУҰ2H2O(g) 2H2(g) +O2(g) ЖҪәвіЈКэKЈҪ Ј»
+O2(g) ЖҪәвіЈКэKЈҪ Ј»
ўЪ№ШУЪТФЙП·ҙУҰЈ¬ПВБРЛө·ЁХэИ·өДКЗ
AЈ® іЈОВПВЈ¬NOЈ¬H2OЈ¬CO2ИэЦЦ»ҜәПОп·ЦҪв·ЕіцСхЖшөДЗгПтҙуРЎЛіРтЈәNOЈҫH2OЈҫCO2 іЈОВПВЈ¬NOЈ¬H2OЈ¬CO2ИэЦЦ»ҜәПОп·ЦҪв·ЕіцСхЖшөДЗгПтҙуРЎЛіРтЈәNOЈҫH2OЈҫCO2 |
| BЈ®ИфЙэёЯОВ¶ИЈ¬·ҙУҰўзөДЖҪәвіЈКэK3Ҫ«Фцҙу |
| CЈ®ИфЦ»ФцјУС№ЗҝЈ¬ЗТ·ҙУҰОпЎўЙъіЙОпЧҙМ¬І»ұдЈ¬·ҙУҰўеЖҪәвІ»·ўЙъТЖ¶ҜЈ¬ЖҪәвіЈКэІ»ұдЈ»·ҙУҰўжЖҪәвіҜХэПтТЖ¶ҜЈ¬ЖҪәвіЈКэФцҙу |
| DЈ®ИфФцјУЖыіө·ў¶Ҝ»ъҝХЖшөДҪшЖшБҝЈ¬ҝЙН¬КұјхЙЩөӘСх»ҜОпәНТ»Сх»ҜМјөДЕЕ·Е |
ИјГә·ПЖшЎўЖыіөОІЖшЦРөДөӘСх»ҜОпЈЁNOxЈ©ЎўТ»Сх»ҜМјөИУРәҰЖшМеЈ¬іЈУГПВБР·Ҫ·ЁҙҰАнЈ¬ТФјхЙЩ¶Ф»·ҫіөДОЫИҫЎЈ
ЈЁ1Ј©¶ФИјГә·ПЖшҪшРРНСПхҙҰАнКұЈ¬іЈАыУГјЧНйҙЯ»Ҝ»№ФӯөӘСх»ҜОпЈ¬ИзЈә
CH4(g)Ј«4NO2(g)ЈҪ4NO(g)Ј«CO2(g)Ј«2H2O(g) ЎчH ЈҪ-574 kJЎӨmol-1
CH4(g)Ј«4NO(g)ЈҪ2N2(g)Ј«CO2(g)Ј«2H2O(g) ЎчH ЈҪ-1160 kJЎӨmol-1
Фт1molCH4Ҫ«NO2»№ФӯОӘN2өД·ҙУҰИИОӘ Ј»
ЈЁ2Ј©іэөӘСх»ҜОпј°COНвЈ¬ЖыіөОІЖшЦР»№ә¬УРМјЗв»ҜәПОпөИОЫИҫОпЈ¬ПВНјКЗЖыіөОІЖшЧӘ»ҜСРҫҝөДКҫТвНјЈәұнКҫөДКЗPt/Al2O3/BaұнГжОьёҪУлҪвОьЧчУГөД»ъАнЈ¬өӘСх»ҜОпКЗNO2Ј¬МјЗв»ҜәПОпКЗCxHyЈ¬РҙіцБҪХЯ·ҙУҰөД»ҜС§·ҪіМКҪЈә Ј¬Pt/Al2O3/BaөДЧчУГКЗ Ј»
ЈЁ3Ј©ЖҪәвіЈКэKөДКэЦөҙуРЎЈ¬КЗәвБҝ»ҜС§·ҙУҰҪшРРіМ¶ИөДұкЦҫЈ¬KөДКэЦөФҪҙ󣬻ҜС§·ҙУҰөДПЮ¶ИФҪҙуЈ¬·ҙУҰОп·ҙУҰөДФҪід·ЦЎЈФЪ25ЎжКұЈ¬ПВБР·ҙУҰөДЖҪәвіЈКэИзПВЈә
N2(g)Ј«O2(g) 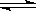 2NO(g) K1ЈҪ1ЎБ10Јӯ30 ўе
2NO(g) K1ЈҪ1ЎБ10Јӯ30 ўе
2H2(g)Ј«O2(g) 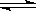 2H2O(g)
K2ЈҪ2ЎБ1081 ўж
2H2O(g)
K2ЈҪ2ЎБ1081 ўж
2CO2 (g) 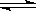 2CO(g)Ј«O2(g) K3ЈҪ4ЎБ10Јӯ92 ўз
2CO(g)Ј«O2(g) K3ЈҪ4ЎБ10Јӯ92 ўз
 ўЩіЈОВПВЈ¬·ҙУҰ2H2O(g)
2H2(g) +O2(g) ЖҪәвіЈКэKЈҪ Ј»
ўЩіЈОВПВЈ¬·ҙУҰ2H2O(g)
2H2(g) +O2(g) ЖҪәвіЈКэKЈҪ Ј»
ўЪ№ШУЪТФЙП·ҙУҰЈ¬ПВБРЛө·ЁХэИ·өДКЗ
AЈ®іЈОВПВЈ¬NOЈ¬H2OЈ¬CO2ИэЦЦ»ҜәПОп·ЦҪв·ЕіцСхЖшөДЗгПтҙуРЎЛіРтЈәNOЈҫH2OЈҫCO2
BЈ®ИфЙэёЯОВ¶ИЈ¬·ҙУҰўзөДЖҪәвіЈКэK3Ҫ«Фцҙу
CЈ®ИфЦ»ФцјУС№ЗҝЈ¬ЗТ·ҙУҰОпЎўЙъіЙОпЧҙМ¬І»ұдЈ¬·ҙУҰўеЖҪәвІ»·ўЙъТЖ¶ҜЈ¬ЖҪәвіЈКэІ»ұдЈ»·ҙУҰўжЖҪәвіҜХэПтТЖ¶ҜЈ¬ЖҪәвіЈКэФцҙу
DЈ®ИфФцјУЖыіө·ў¶Ҝ»ъҝХЖшөДҪшЖшБҝЈ¬ҝЙН¬КұјхЙЩөӘСх»ҜОпәНТ»Сх»ҜМјөДЕЕ·Е
ўЫ»щУЪ»·ұЈ·Ё№жЈ¬ТӘЗуёДЧ°ЖыіөОІЖшҙҰАнЧ°ЦГЈ¬ҙпөҪК№өӘСх»ҜОпЈЁNOЈ©ЎўТ»Сх»ҜМјЧӘ»ҜОӘОЮОЫИҫЎўҝЙЕЕ·ЕөДЖшМеөДДҝөДЎЈёДЧ°өД·Ҫ·ЁЦчТӘКЗјУИлУРР§ҙЯ»ҜјБЈ¬ЗлДгёщҫЭТФЙПУР№ШКэҫЭ·ЦОцЈ¬ФЪІ»ёДұдЖдЛьМхјюөДЗйҝцПВЈ¬ҝЙК№УГҙЯ»ҜјБіэОЫИҫЖшМеөДФӯТтЈә ЎЈ
°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com