(2011?四川二模)许多含氯物质与生活密切相关,如HClO、ClO
2、NaClO
2等都是重要的杀菌消毒剂和漂白剂.下列是重要的含氯漂白剂NaClO
2的工业合成流程图.
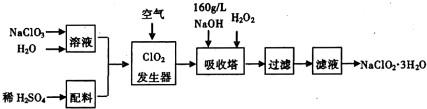
已知:纯ClO
2易炸,当空气中ClO
2的浓度大于10%容易爆炸.回答下列问题
:(1)在碱性溶液中NaClO
2比较稳定,所以吸收塔中应维持NaOH稍过量,判断NaOH是否过量的简单实验方法是
用pH试纸检验溶液的pH
用pH试纸检验溶液的pH
;
(2)吸收塔中为防止NaClO
2被还原成NaCl,所用还原剂的还原性应适中,除用H
2O
2外,还可以选择的还原剂是
a
a
;(填代号)
a.Na
2O
2 b.Na
2S c.FeCl
2 d.铁粉
(3)能否将ClO
2气体用SO
2气体稀释
否
否
(填“能“或“否“),理由是
SO2能与ClO2、NaOH、H2O2发生化学反应
SO2能与ClO2、NaOH、H2O2发生化学反应
;
(4)NaClO
2溶液与FeCl
2溶液相遇,有大量红褐色沉淀产生,该反应的离子方程式为
3ClO2-+12Fe2++6H2O=4Fe(OH)3↓+3Cl-+8Fe3+
3ClO2-+12Fe2++6H2O=4Fe(OH)3↓+3Cl-+8Fe3+
;
(5)为了测定NaClO
2?3H
2O的纯度,取上述合成产品10g溶于水配成500mL溶液,取出10mL溶液于锥形瓶中,再加入足量酸化的KI溶液,充分反应后加入2~3滴淀粉溶液,用0.264mol/L Na
2S
2O
3标准液滴定,锥形瓶中溶液
蓝色变为无色
蓝色变为无色
(填颜色变化),且半分钟内不发生变化,说明滴定达终点,用去标准液20.00mL,试样纯度是否合格
合格
合格
(填“合格”或“不合格”,合格纯度在90%以上).提示:2Na
2S
2O
3+I
2═Na
2S
4O
6+2NaI.