
题目列表(包括答案和解析)
室温下,向一定体积的密闭容器中充入干燥的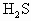 气体m
mL和
气体m
mL和 气体n
mL,在未发生反应前容器内压强为 P,反应后,在相同温度下,容器内气体压强变为
气体n
mL,在未发生反应前容器内压强为 P,反应后,在相同温度下,容器内气体压强变为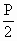 ,求反应前
,求反应前 的体积比.
的体积比.
室温下,将 4 mol A 气体和 2 mol B 气体在 2 L 的密闭容器中混合并在一定条件下发生如下反应:2A(气)+B(气)![]() XC(气),经 2 s(秒)后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为 1.4 mol,现有下列几种说法:
XC(气),经 2 s(秒)后反应达平衡,测得 C 的浓度为 0.6 mol·L-1 ,B的物质的量为 1.4 mol,现有下列几种说法:
① 用物质 A 表示的反应的平均速率为 0.3 mol·L-1·s-1
② 反应前容器内的压强与平衡后容器内的压强之比为1:1
③ 2 s 时物质A的转化率为30%
④ X=2
⑤ 室温下该反应的化学反应平衡常数是0.5
⑥其他条件不变,向容器中再加入1 molC气体,达到新平衡时,C的体积分数不变
其中正确的是( )
A.①③④ B.①④⑥ C.②③⑤ D.③⑤⑥
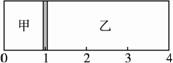
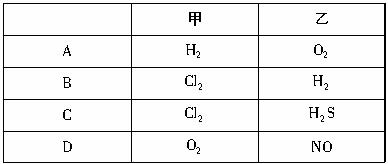
(14分)(1)在一定温度下,向1L体积固定的密闭容器中加入1mol A(g),发生反应2A(g) B(g)+C(g),B的物质的量随时间的变化如图所示。 0—2min内的平均反应速率v(A)= . 相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时 是原来的2倍。
B(g)+C(g),B的物质的量随时间的变化如图所示。 0—2min内的平均反应速率v(A)= . 相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时 是原来的2倍。
a.平衡常数 b. A的平衡浓度
c.平衡时混合气体的密度 d.平衡时B的体积分数
(2)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡 移动(填“向左”“向右”或“不”);若加入少量下列试剂中的 ,产生H2的速率将增大。
a.NaNO3 b.CuSO4
c.Na2SO4 d.NaHSO3
e. CH3COOH
(3)用惰性电极电解Cu(NO3)2溶液一段时间后,加入a mol 的Cu(OH)2可使溶液恢复原状,则电解过程中转移的电子数目为_____________
(4)已知:2Zn(s)+O2(g)=2ZnO(s) △H=-701.0kJ·mol-1
2Hg(l)+O2(g)=2HgO(s) △H=-181.6kJ·mol-1
则反应Zn(s)+ HgO(s)=ZnO(s)+ Hg(l) △H=_____________
(5)已知25℃时,Ksp[Cu(OH)2]=2×10-20,要使0.2 mol·L-1 CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为 。
(14分)(1)在一定温度下,向1L体积固定的密闭容器中加入1mol A(g),发生反应2A(g) B(g)+C(g),B的物质的量随时间的变化如图所示。 0—2min内的平均反应速率v(A)= .
相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时 是原来的2倍。
B(g)+C(g),B的物质的量随时间的变化如图所示。 0—2min内的平均反应速率v(A)= .
相同温度下,若开始加入A(g)的物质的量是原来的2倍,则平衡时 是原来的2倍。
a.平衡常数 b. A的平衡浓度
c.平衡时混合气体的密度 d.平衡时B的体积分数
(2)实验室用Zn和稀硫酸制取H2,反应时溶液中水的电离平衡 移动(填“向左”“向右”或“不”);若加入少量下列试剂中的 ,产生H2的速率将增大。
a.NaNO3 b.CuSO4
c.Na2SO4 d.NaHSO3
e. CH3COOH
(3)用惰性电极电解Cu(NO3)2 溶液一段时间后,加入a mol 的Cu(OH)2可使溶液恢复原状,则电解过程中转移的电子数目为_____________
(4)已知:2Zn(s)+O2(g)=2ZnO(s) △H=-701.0kJ·mol-1
2Hg(l)+O2(g)=2HgO(s) △H=-181.6kJ·mol-1
则反应Zn(s)+ HgO(s)=ZnO(s)+ Hg(l) △H=_____________
(5)已知25℃时,Ksp[Cu(OH)2]=2×10-20,要使0.2 mol·L-1 CuSO4溶液中Cu2+沉淀较为完全(使Cu2+浓度降至原来的千分之一),则应向溶液里加入NaOH溶液,使溶液的pH为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com