
题目列表(包括答案和解析)
(08龙岩一中二模)(13分)A、B、C、D、E、F均为短周期元素,A能与E形成气态AE4,其中A的质量分数为75%,E与B能形成常温呈液态的E2B型化合物,C的最高价氧化物的水化物是酸性最强的酸,D在地壳中含量仅次于B,E既能形成单原子核的阳离子,又能生成单原子核的阴离子,F是短周期中原子半径最大的原子(除稀有气体).
 (1)工业制取D单质的化学方程式为
(1)工业制取D单质的化学方程式为
(2)一小粒F单质放在石棉网上加热,反应的现象是
(3)AE4是含有 键(填化学键类型)的 分子(填 极性,非极性)。
(4)C单质和石灰乳反应的化学方程式为 ;
一满烧瓶C单质的水溶液如图倒置于水槽中较长时间日照后,在瓶底积蓄一定量的气体,检验该气体的操作是
。
(5)7.8克F2B2和过量的E2B反应时转移的电子数为 NA(NA为阿伏加德罗常数的值)
有a gKCl 不饱和溶液,其质量分数为c%,采取措施后使其变为饱和溶液b g,溶质质量分数为d%,下列说法正确的是( )
A、a不可能等于b B、a•c%一定等于 b•d%
C、原条件下KCl的溶解度大于c g D、c%一定小于d%
第Ⅱ卷(非选择题 共52分)
非选择题 【共道小题,分】【14分】下图是实验室验证某铜银合金完全溶解于一定量的浓硝酸时,生成NO2气体中含有NO的实验装置。常温下,NO2与N2O4混合存在,在低于0 ℃时,几乎只有白色N2O4晶体存在。
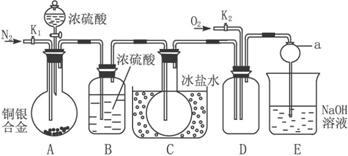
(1)反应前打开A部分的活塞K1,持续通一段时间氮气,其理由是_____________________
_____________________________________________________________________。
(2)若装置中缺B部分,其后果是__________________________________________________。
(3)反应结束后,打开D部分的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色;若通入的是热的氧气,则瓶内气体的颜色比前者更深,其原因是__________________________。
(4)E部分中a仪器所起的作用是______________________________________________。
(5)已知该铜银合金的质量为15 g,加入40 mL 135 mol·L-1的浓硝酸,实验结束后,A部分烧瓶内溶液中的c(H+)=1 mol·L-1(假设反应中HNO3既无挥发也无分解,体积仍为40 mL)。
①参加反应硝酸的物质的量为_____________________。
②为测定铜银合金中铜的质量分数,还需要进行的主要实验操作是_____________________。
700℃时,向容积为2L的密闭容器中充入一定量的CO和H2O,发生反应:
CO(g)+H2O(g)  CO2+H2(g)
CO2+H2(g)
反应过程中测定的部分数据见下表(表中t1>t2):
|
反应时间/min |
n(CO)/mol |
H2O/ mol |
|
0 |
1.20 |
0.60 |
|
t1 |
0.80 |
|
|
t2 |
|
0.20 |
下列说法正确的是
A.反应在t1min内的平均速率为
B.保持其他条件不变,起始时向容器中充入0.60molCO和1.20 molH2O,到达平衡时
C.保持其他条件不变,向平衡体系中再通入0.20molH2O,与原平衡相比,达到新平衡时CO转化率增大,H2O的体积分数增大
D.温度升至800℃,上述反应平衡常数为0.64,则正反应为吸热反应
非选择题
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com