
题目列表(包括答案和解析)

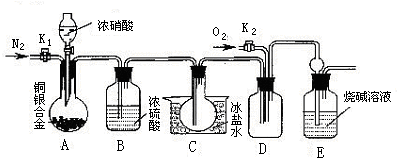

(1)反应前先打开A中的活塞K1,持续通一段时间N2,其理由是___________________。
(2)若装置中缺B,其后果是_______________________。
(3)反应结束后,打开D中的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色,反应的化学方程式为________________________;若通入的是热氧气,则瓶内气体的颜色比以前更深,其原因是____________________________________。(用方程式和必要的文字说明)
(4)C装置的作用是_______________________________________________________;
E中a仪器所起的作用是___________________________________________________。
(5)为测定该银圆中银的质量分数,还需进行的主要实验操作是:将A中溶液倒入烧杯中,然后加入过量的NaCl溶液,随后进行的操作为____________(用ABCD字母排序),最后测定溶液中Ag+的质量。
A.洗涤 B.过滤 C.称量 D.烘干
(11分)下图为某实验者设计的验证银圆(银和铜的合金)完全溶解于一定量的浓硝酸后生成NO2气体中含有NO的实验装置图。常温时,NO2与N2O4同时存在;在低于0℃时,几乎只有无色的N2O4的晶体存在。

(1)反应前先打开A中的活塞K1,持续通一段时间N2,其理由是 。
(2)若装置中缺B,其后果是 。
(3)反应结束后,打开D中的活塞K2,并通入氧气,D瓶内气体由无色变为红棕色;若通入的是热氧气,则瓶内气体的颜色比以前更深,其原因是 。
(4)C装置的作用是 ;E中a仪器所起的作用是 。
(5)已知该银圆的质量为25g,加入75mL 12mol·L—1的浓硝酸。实验结束后,A中烧瓶内溶液中H+的浓度为2mol·L—1(反应中HNO3既无挥发也无分解),溶液体积仍为75mL。
①参加反应的硝酸的物质的量是 。
②为测定该银圆中铜的质量分数,还需进行的主要实验操作是 。
欲用浓硝酸法测定某铜银合金中铜的质量分数(测定反应后生成气体的量),但资料表明:①反应中除生成NO2气体外还有少量NO生成;②常温下NO2和N2O4混合存在,在低于0℃时,几乎只有无色的N2O4液体或晶体存在。为完成测定并验证确有NO生成,有人设计了如图所示的实验装置。
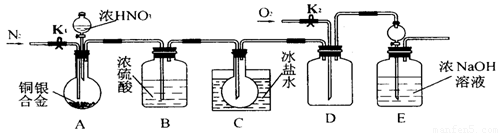
(1)实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是__________________________。
(2)装置中B瓶的作用是 。
(3)A中的反应停止后,打开D中的活塞K2,并通入氧气,若反应确有NO产生,则D中应出现的现象是_____________。
(4)为减少测量误差,在A中反应完成和D中出现现象后,还应继续进行的操作是___________。
(5)C装置烧瓶中的物质是 ,用简单的实验证实你的判断: 。
(6)实验已测出一定质量的铜银合金完全反应后E装置的生成物中含氮元素的质量,为确定合金中铜的质量分数还需测定的数据是______________________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com