
题目列表(包括答案和解析)

| 实验操作 | 实验现象 | 结论 | 相应的离子方程式 |
| 取少量晶体于试管中,充分加热 | 试管内有固体剩余 | ______ | ______ |
| ______ | 固体全部溶解,有气泡产生 | ______ | ______ |
| 实验操作 | 实验现象 | 结论 | 相应的离子方程式 |
| 取少量晶体于试管中,充分加热 | 试管内有固体剩余 | ______ | ______ |
| ______ | 固体全部溶解,有气泡产生 | ______ | ______ |
已知甲、乙、丙均为常见气体,其中甲在空气中含量最多,乙在相同条件下密度最小,丙有刺激性气味,且一个丙分子由四个原子构成。
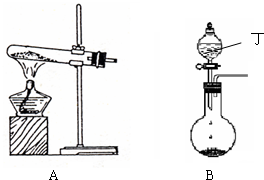
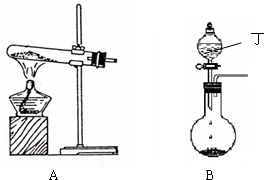
(1)实验室中可用下图A或B装置与相应的药品制得丙。
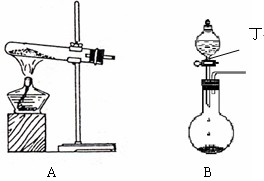
① A中试管内反应的化学方程式是 。
② B中分液漏斗内盛放的物质丁是 ,圆底烧瓶内的物质是 。(均填名称)
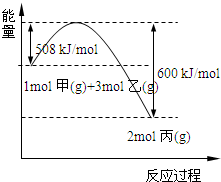
(2)工业上将甲和乙在高温、高压、催化剂的条件下制取丙。下图是甲和乙反应过程中能量变化图:
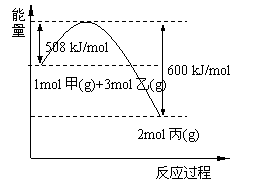 |
该反应的热化学方程式是 。
(3)丙在氧气中燃烧的反应是置换反应,该反应的化学方程式是 。
(4)① 将丙和CO2气体通入饱和食盐水中有碳酸氢钠晶体析出,反应的离子方程式是 。
②为了验证上述晶体既不是NH4HCO3、也不是NaCl而是NaHCO3,设计实验方案如下,完成下列部分实验报告:
实验操作 | 实验现象 | 结论 | 相应的离子方程式 |
取少量晶体于试管中,充分加热 | 试管内有固体剩余 |
|
|
| 固体全部溶解,有气泡产生 |
|
|
(5)若用(1)中得A制取丙,并用园底烧瓶通过排气法收集丙(标准状况),然后进行喷泉实验。当水进入到烧瓶体积得3/5时,液面不再上升,此时立即关闭止水夹,烧瓶内溶液中溶质的物质的量浓度是 mol/L(精确0.001)。
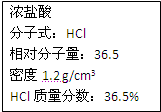 右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:(15分)右图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
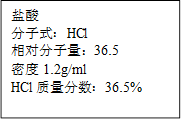
(1)该浓盐酸中HCl的物质的量浓度为 mol/L。
(2)取用任意体积的该盐酸溶液时,下列物理量中不随所取
体积的多少而变化的是 。
A.溶液中HCl的物质的量 B.溶液的浓度
C.溶液中Cl-的数目 D.溶液的密度
(3)某学生欲用上述浓盐酸和蒸馏水配制500 mL物质的量浓度为0.3 mol/L稀盐酸。
①该学生需要量取 mL上述浓盐酸进行配制。
②配制过程中,需要使用的仪器是(填写代号)________。
A.烧杯 B.量筒 C.1000 mL容量瓶 D.托盘天平
E.药匙 F.500 mL容量瓶 G.胶头滴管 H.玻璃棒
③配制时,其正确的操作顺序是(字母表示,每个字母只能用一次) ;
A.用30mL水洗涤烧杯2—3次,洗涤液均注入容量瓶,振荡
B.用量筒准确量取所需浓盐酸的体积,慢慢沿杯壁注入盛有少量水(约30mL)的烧杯中,用玻璃棒慢慢搅动,使其混合均匀
C.将已冷却的盐酸沿玻璃棒注入500mL的容量瓶中
D.将容量瓶盖紧,颠倒摇匀
E.改用胶头滴管加水,使溶液凹面恰好与刻度线相切
F.继续往容量瓶内小心加水,直到液面接近刻度线1—2cm处
④在配制过程中,下列实验操作会使所配制的稀盐酸的物质的量浓度偏高的是
A.用量筒量取浓盐酸时俯视观察凹液面
B.溶液注入容量瓶前没有恢复到室温就进行定容
C.定容时仰视刻度线
D.在配置前用已知浓度的稀盐酸润洗容量瓶
(4)若在标准状况下,将VLHCl气体溶于1L水中,所得溶液密度为dg/mL,则此溶液的物质的量浓度为 mol/L。
(5)现将100mL0.5mol/L的盐酸200mL0.1mol/LCuCl2溶液混合,体积变化忽略不计,所得溶液中Cl-的物质的量浓度是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com