
МвДҝБРұн(°ьАЁҙр°ёәНҪвОц)
H2(g)+ ![]() O2(g)
O2(g)![]() H2O(l) ҰӨH=-285.8 kJЎӨmol-1
H2O(l) ҰӨH=-285.8 kJЎӨmol-1
C3H8(g)+5O2(g)![]() 3CO2(g)+4H2O(l) ҰӨH=-2 220.0 kJЎӨmol-1
3CO2(g)+4H2O(l) ҰӨH=-2 220.0 kJЎӨmol-1
КөСйІвөГЗвЖшәНұыНйөД»мәПЖшМе№І5 molЈ¬НкИ«ИјЙХКұ·ЕИИ3 847 kJ,Фт»мәПЖшМеЦРЗвЖшәНұыНйөДМе»эұИКЗ__________Ј»БҪХЯ·ЕіцөДИИБҝЦ®ұИФјОӘ__________ЎЈ
A.1ЎГ3 B.3ЎГ1 C.1ЎГ4 D.5ЎГ13
H2(g)+![]() O2(g)====H2O(l)Ј»ҰӨH=-285.8 kJЎӨmol-1
O2(g)====H2O(l)Ј»ҰӨH=-285.8 kJЎӨmol-1
C3H8(g)+5O2(g)====3CO2(g)+4H2O(l)Ј»ҰӨH=-2220 kJЎӨmol-1
КөСйІвөГH2әНC3H8өД»мәПЖшМе№І5 molЈ¬НкИ«ИјЙХКұ·ЕИИ3847 kJЈ¬Фт»мәПЖшМеЦРH2УлC3H8өДМе»эұИКЗ( )
A.1ЎГ1 B.1ЎГ3 C.3ЎГ1 D.1ЎГ4
ЈЁ1Ј©ЈЁ4·ЦЈ©ПВНјұнКҫФЪГЬұХИЭЖчЦР·ҙУҰЈә2SO2+O22SO3 ЎчH<0ҙпөҪЖҪәвКұЈ¬УЙУЪМхјюёДұд¶шТэЖр·ҙУҰЛЩ¶ИәН»ҜС§ЖҪәвөДұд»ҜЗйҝцЈ¬ab№эіМЦРёДұдөДМхјюҝЙДЬКЗ Ј»bc№эіМЦРёДұдөДМхјюҝЙДЬКЗ Ј»
ЈЁ2Ј©ЈЁ3·ЦЈ©ТСЦӘПВБРБҪёцИИ»ҜС§·ҪіМКҪЈә
H2(g)Ј«O2(g) ЈҪ H2O(l ) ЎчHЈҪЈӯ285.8 kJЎӨmolЈӯ1
C3H8(g)Ј«5O2(g) ЈҪ 3CO2(g)+4H2O(l) ЎчHЈҪЈӯ2220.2 kJЎӨmolЈӯ1
КөСйІвөГH2әНC3H8өД»мәПЖшМе№І5molЈ¬НкИ«ИјЙХЙъіЙТәМ¬Л®Кұ·ЕИИ3847kJЈ¬Фт»мәПЖшМеЦРH2әНC3H8өДМе»эұИКЗ
ЈЁ3Ј©ЎўЈЁ3·ЦЈ©КөСйКТҪшРРөзҪвВИ»ҜДЖИЬТәКұЈ¬БҪј«№ІКХјҜөҪ4.48LЖшМеЈЁұкҝцЈ©Ј¬јЩЙи·ҙУҰәуИЬТәөДЧЬМе»эОӘ200mlЈ¬ФтөзҪвәуИЬТәЦРЗвСх»ҜДЖөДОпЦКөДБҝЕЁ¶И
ЈЁ1Ј©ЈЁ4·ЦЈ©ПВНјұнКҫФЪГЬұХИЭЖчЦР·ҙУҰЈә2SO2+O2 2SO3 ЎчH<0ҙпөҪЖҪәвКұЈ¬УЙУЪМхјюёДұд¶шТэЖр·ҙУҰЛЩ¶ИәН»ҜС§ЖҪәвөДұд»ҜЗйҝцЈ¬ab№эіМЦРёДұдөДМхјюҝЙДЬКЗ Ј»bc№эіМЦРёДұдөДМхјюҝЙДЬКЗ Ј»
2SO3 ЎчH<0ҙпөҪЖҪәвКұЈ¬УЙУЪМхјюёДұд¶шТэЖр·ҙУҰЛЩ¶ИәН»ҜС§ЖҪәвөДұд»ҜЗйҝцЈ¬ab№эіМЦРёДұдөДМхјюҝЙДЬКЗ Ј»bc№эіМЦРёДұдөДМхјюҝЙДЬКЗ Ј»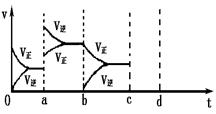
ЈЁ2Ј©ЈЁ3·ЦЈ©ТСЦӘПВБРБҪёцИИ»ҜС§·ҪіМКҪЈә
H2(g)Ј« O2(g) ЈҪ H2O( l ) ЎчHЈҪЈӯ285.8 kJЎӨmolЈӯ1
O2(g) ЈҪ H2O( l ) ЎчHЈҪЈӯ285.8 kJЎӨmolЈӯ1
C3H8(g)Ј«5O2(g) ЈҪ 3CO2(g) +4H2O(l) ЎчHЈҪЈӯ2220.2 kJЎӨmolЈӯ1
КөСйІвөГH2әНC3H8өД»мәПЖшМе№І5molЈ¬НкИ«ИјЙХЙъіЙТәМ¬Л®Кұ·ЕИИ3847kJЈ¬Фт»мәПЖшМеЦРH2әНC3H8өДМе»эұИКЗ
ЈЁ3Ј©ЎўЈЁ3·ЦЈ©КөСйКТҪшРРөзҪвВИ»ҜДЖИЬТәКұЈ¬БҪј«№ІКХјҜөҪ4.48LЖшМеЈЁұкҝцЈ©Ј¬јЩЙи·ҙУҰәуИЬТәөДЧЬМе»эОӘ200mlЈ¬ФтөзҪвәуИЬТәЦРЗвСх»ҜДЖөДОпЦКөДБҝЕЁ¶И
 2SO3 ЎчH<0ҙпөҪЖҪәвКұЈ¬УЙУЪМхјюёДұд¶шТэЖр·ҙУҰЛЩ¶ИәН»ҜС§ЖҪәвөДұд»ҜЗйҝцЈ¬ab№эіМЦРёДұдөДМхјюҝЙДЬКЗ Ј»bc№эіМЦРёДұдөДМхјюҝЙДЬКЗ Ј»
2SO3 ЎчH<0ҙпөҪЖҪәвКұЈ¬УЙУЪМхјюёДұд¶шТэЖр·ҙУҰЛЩ¶ИәН»ҜС§ЖҪәвөДұд»ҜЗйҝцЈ¬ab№эіМЦРёДұдөДМхјюҝЙДЬКЗ Ј»bc№эіМЦРёДұдөДМхјюҝЙДЬКЗ Ј»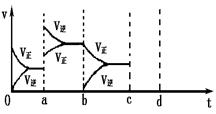
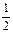 O2(g) ЈҪ H2O( l ) ЎчHЈҪЈӯ285.8 kJЎӨmolЈӯ1
O2(g) ЈҪ H2O( l ) ЎчHЈҪЈӯ285.8 kJЎӨmolЈӯ1°Щ¶ИЦВРЕ - Б·П°ІбБРұн - КФМвБРұн
әюұұКЎ»ҘБӘНшОҘ·ЁәНІ»БјРЕПўҫЩұЁЖҪМЁ | НшЙПУРәҰРЕПўҫЩұЁЧЁЗш | өзРЕХ©ЖӯҫЩұЁЧЁЗш | ЙжАъК·РйОЮЦчТеУРәҰРЕПўҫЩұЁЧЁЗш | ЙжЖуЗЦИЁҫЩұЁЧЁЗш
ОҘ·ЁәНІ»БјРЕПўҫЩұЁөз»°Јә027-86699610 ҫЩұЁУКПдЈә58377363@163.com