
题目列表(包括答案和解析)
(15分)现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍。X原子的M能层上有4个未成对电子。请回答下列问题:
(1)写出C、D、E三种原子第一电离能由大到小的顺序为_______________。
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为_____________,根据价层电子对互斥理论预测BA2D的分子构型为____________。
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个BC-。与A同族且相差两个周期的元素R的离子位于立方体的恰当位置上。根据其结构特点可知该晶体的化学式为(用最简正整数表示)________
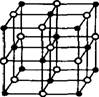
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ·mol-1 | 786 | 715 | 3401 |
根据表格中的数据:判断KCl、MgO、TiN 三种离子晶体熔点从高到低的顺序是______________。MgO晶体中一个Mg2+周围和它最邻近且等距离的O2-有__________________个。
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是__________________。
(15分)现有前四周期A、B、C、D、E、X六种元素,已知B、C、D、E、A五种非金属元素原子半径依次减小,其中B的s能级上电子总数等于p能级上电子总数的2倍。X原子的M能层上有4个未成对电子。请回答下列问题:
(1)写出C、D、E三种原子第一电离能由大到小的顺序为_______________。
(2)A原子与B、C、D原子形成最简单化合物的稳定性由强到弱的顺序为_____________,根据价层电子对互斥理论预测BA2D的分子构型为____________。
(3)某蓝色晶体,其结构特点是X2+、X3+离子分别占据立方体互不相邻的顶点,而立方体的每条棱上均有一个BC-。与A同族且相差两个周期的元素R的离子位于立方体的恰当位置上。根据其结构特点可知该晶体的化学式为(用最简正整数表示)________
(4)科学家通过X射线探明,KCl、MgO、CaO、TiN的晶体结构与NaCl的晶体结构相似(如图所示),其中3种离子晶体的晶格能数据如下表:
|
离子晶体 |
NaCl |
KCl |
CaO |
|
晶格能/kJ·mol-1 |
786 |
715 |
3401 |
根据表格中的数据:判断KCl、MgO、TiN 三种离子晶体熔点从高到低的顺序是______________。MgO晶体中一个Mg2+周围和它最邻近且等距离的O2-有__________________个。
(5)研究物质磁性表明:金属阳离子含未成对电子越多,则磁性越大,磁记录性能越好。离子型氧化物V2O5和Cr2O3中,适合作录音带磁粉原料的是__________________。
(15分) 回答如下几个问题
(1)近期发现不需要外加能源、节约水源而能除去废水中的卤代烷(有碍于人类健康)的方法:把铁放在含卤代烷的废水中,经一段时间后卤代烷“消失”。例如废水中的一氯乙烷经14.9d后就检不出来了。目前认为反应中卤代烷(RCH2X)是氧化剂。写出反应式并说明(按原子)得失电子的关系。
(2) 电解NaCl―KCl―AlCl3熔体制铝比电解Al2O3―Na3AlF6制铝节省电能约30%。为什么现仍用后一种方法制铝?
(3) NH4NO3热分解及和燃料油[以(CH2)n表示]反应的方程式及反应热分别为:
NH4NO3 = N2O + 2H2O + 0.53 kJ/g NH4NO3 …………(1)
NH4NO3 = N2 + 1/2 O2 + 2H2O + 1.47 kJ/g NH4NO3 ………(2)
3n NH4NO3 + (CH2)n = 3n N2 + 7n H2O + n CO2 + 4.29n kJ/g NH4NO3 ……(3)
试问:由以上三个热化学方程式可得出哪些新的热化学方程式?
(4) 参照水溶液化学反应的知识回答下面的问题:在液态BrF3中用KBrF4滴定Br2PbF10,过程中出现电导最低点。写出有关反应式。
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ?mol-1 | 786 | 715 | 3401 |
回答如下几个问题
(1)近期发现不需要外加能源、节约水源而能除去废水中的卤代烷(有碍于人类健康)的方法:把铁放在含卤代烷的废水中,经一段时间后卤代烷“消失”。例如废水中的一氯乙烷经14.9d后就检不出来了。目前认为反应中卤代烷(RCH2X)是氧化剂。写出反应式并说明(按原子)得失电子的关系。
(2) 电解NaCl—KCl—AlCl3熔体制铝比电解Al2O3—Na3AlF6制铝节省电能约30%。为什么现仍用后一种方法制铝?
(3) NH4NO3热分解及和燃料油[以(CH2)n表示]反应的方程式及反应热分别为:
NH4NO3 = N2O + 2H2O + 0.53 kJ/g NH4NO3 …………(1)
NH4NO3 = N2 + 1/2 O2 + 2H2O + 1.47 kJ/g NH4NO3 ………(2)
3n NH4NO3 + (CH2)n = 3n N2 + 7n H2O + n CO2
+ 4.29n kJ/g NH4NO3 ……(3)
试问:由以上三个热化学方程式可得出哪些新的热化学方程式?
(4) 参照水溶液化学反应的知识回答下面的问题:在液态BrF3中用KBrF4滴定Br2PbF10,过程中出现电导最低点。写出有关反应式。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com