
题目列表(包括答案和解析)
在元素周期表中,一稀有气体元素原子的最外层电子构型为4s24p6,与其同周期的A、B、C、D四种元素,它们原子的最外层电子数依次为2、2、1、7,其中A、C两元素原子的次外层电子数为8,B、D两元素原子的次外层电子数为18,E、D两元素处于同族,且在该族元素种,E的气态氢化物的沸点最高;E、F、G、H四种元素处于同一周期,F的最高价氧化物对应的水化物酸性在同周期中是最强的,G的电负性介于E、F之间,H、F相邻。回答下列问题:
⑴写出下列元素符号B___________,H___________。
⑵A、C、D三元素形成的简单离子的半径由大到小的顺序是(写离子符号)___________。
⑶E、F、G三元素的第一电离能由大到小的顺序是(写元素符号)___________。
⑷D元素所在周期的元素种数为___________,所在族的价电子的电子排布式___________。
⑸F元素的气态氢化物分子的空间构型是___________,中心原子的杂化类型是___________。
⑹H和F形成一种超硬、耐磨、耐高温的新型化合物,该化合物属于___________晶体,其硬度比金刚石___________(填“大”或“小” )。
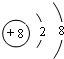






湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com