
题目列表(包括答案和解析)
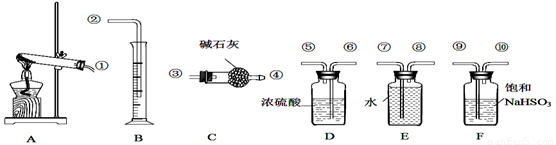
硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同。气体成分可能含SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式。实验用到的仪器如右图所示:
【提出假设】
Ⅰ.所得气体的成分可能只含_________一种;
Ⅱ.所得气体的成分可能含有____________________二种;
Ⅲ.所得气体的成分可能含有SO2、SO3、O2三种。
【实验探究】实验操作过程(略)已知实验结束时,硫酸铜完全分解。
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为①⑨⑩______________(填序号、仪器不重复使用)。
(2)实验过程中,仪器F的作用是 。
【验证假设,分析推理】
(3)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同.数据如下:
|
实验 小组 |
称取无水CuSO4的质量/g |
仪器C增加的质量/g |
量筒中水的体积折算标准状况下气体的体积/mL |
|
① |
6.4 |
2.56 |
224 |
|
② |
6.4 |
2.56 |
448 |
请通过计算,推断出第②小组CuSO4分解的化学反应方程式: 。
若将①小组CuSO4分解时所得气体在一定条件下反应并达到平衡,恢复到反应前的温度和压强时,测得密度是反应前的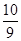 ,其平衡常数表达式为
最终所得气体的平均相对分子质量为__________(保留一位小数)
,其平衡常数表达式为
最终所得气体的平均相对分子质量为__________(保留一位小数)
硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同。气体成分可能含SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式。实验用到的仪器如右图所示:
【提出假设】
Ⅰ.所得气体的成分可能只含_________一种;
Ⅱ.所得气体的成分可能含有____________________二种;
Ⅲ.所得气体的成分可能含有SO2、SO3、O2三种。
【实验探究】实验操作过程(略)已知实验结束时,硫酸铜完全分解。
(1)请你组装探究实验的装置,按从左至右的方向,各仪器接口连接顺序为①⑨⑩______________(填序号、仪器不重复使用)。
(2)实验过程中,仪器F的作用是 。
【验证假设,分析推理】
(3)有两个实验小组进行该实验,由于加热时的温度不同,实验结束后测得相关数据也不同.数据如下:
| 实验 小组 | 称取无水CuSO4的质量/g | 仪器C增加的质量/g | 量筒中水的体积折算标准状况下气体的体积/mL |
| ① | 6.4 | 2.56 | 224 |
| ② | 6.4 | 2.56 | 448 |
 ,其平衡常数表达式为 最终所得气体的平均相对分子质量为__________(保留一位小数)
,其平衡常数表达式为 最终所得气体的平均相对分子质量为__________(保留一位小数) 硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同.气体成分可能含SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式.实验用到的仪器如图所示:
硫酸铜受热分解生成氧化铜和气体,受热温度不同,该气体成分也不同.气体成分可能含SO2、SO3和O2中的一种、二种或三种.某化学课外活动小组通过设计一探究性实验,测定反应产生的SO2、SO3和O2的物质的量,并经计算确定各物质的化学计量数,从而确定CuSO4分解的化学方程式.实验用到的仪器如图所示:| 实验 小组 | 称取CuSO4 的质量/g | 仪器C增 加的质量/g | 量筒中水的体积折算标 准状况下气体的体积/mL |
| ① | 6.4 | 2.56 | 224 |
| ② | 6.4 | 2.56 | 448 |
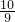 ,则最终所得气体的平均相对分子质量为______(保留一位小数);指导老师认为利用上述装置测得的仪器C增重量偏小,他的理由可能是______.
,则最终所得气体的平均相对分子质量为______(保留一位小数);指导老师认为利用上述装置测得的仪器C增重量偏小,他的理由可能是______.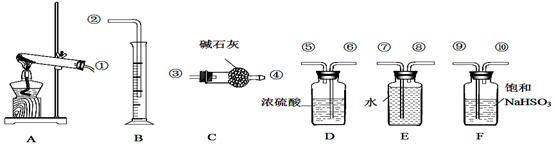
| 实验 小组 | 称取无水CuSO4的质量/g | 仪器C增加的质量/g | 量筒中水的体积折算标准状况下气体的体积/mL |
| ① | 6.4 | 2.56 | 224 |
| ② | 6.4 | 2.56 | 448 |
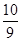 ,其平衡常数表达式为 最终所得气体的平均相对分子质量为__________(保留一位小数)
,其平衡常数表达式为 最终所得气体的平均相对分子质量为__________(保留一位小数)(14分)欲用浓硝酸法(测定反应后生成气体的量)测定某铜银合金中铜的质量分数。资料表明:①反应中除生成NO2气体外还有少量的NO生成;②常温下N02与N2O4混合存在,在低于0℃时几乎只有无色N2O4液体或晶体存在。为完成测定并验证有NO生成,有人设计下图实验装置。
(1)实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是________________________________________________。
(2)装置B瓶的作用是___________________________________________。
(3)A中反应停止后,打开D中的活塞K2并通人氧气,若反应中确有NO产生,则D中应出现的现象是________________;实验发现,通人氧气温度的高低对实验现象有较大影响,则为了便于观察应通人_______________(填“冷”或“热”)的氧气。
(4)为了减少测量误差,在A中反应完成和D中出现现象后,还应继续进行的操作是:___________________________________________________。
(5)实验测得下列数据:所用铜银合金质量为15.0 g,浓硝酸的体积为40 mL,浓度为13.5mol·L-1。实验后:A中溶液体积为40mL,H+浓度为1.0mol·L-1。若设反应中硝酸既无挥发也无分解,则:
①参加反应的硝酸的物质的量为______________;
②若已测出反应后E装置的生成物含氮元素的质量,则为确定合金中铜的质量分数,还需要测定的数据是__________。
(6)实验中只测定铜的质量分数,不验证NO的产生,则在铜银合金与硝酸反应后,只需简单的实验操作就可以达到目的,请简述实验过程_______________ ____。
【解析】本实验的目的有两个。一是验证反应中除生成NO2气体外还有少量的NO生成,二是测定某铜银合金中铜的质量分数,解题时我们始终围绕这两个目的。要验证有NO生成,就必须要保证整个装置中没有氧气存在,否则即使生成NO,也会转变成NO2,所以实验开始前要先打开A部分的活塞K1,持续通一段时间的氮气再关闭K1,这样做的目的是排尽装置中的空气。检验NO的方法是将NO与O2反应生成红棕色的NO2,由于反应中本来就生成NO2,所以必须将NO2与NO分离,结合题目不难得到装置C的作用就是将NO2转变成无色N2O4液体或晶体。如果温度过低NO2会转变成无色N2O4液体或晶体,所以为了便于观察应通人热的氧气。要测定某铜银合金中铜的质量分数除知道铜银合金的质量外,还必须测得与铜银合金相关的另外一个量,方可列方程组求解。结合题意,可知方法为测出氮的氧化物的质量。由于氮的氧化物存在于C、E两个装置中,所以必须测出两个装置的质量变化。另为保证测定准确,在A中反应完成和D中出现现象后,还应打开K1、K2,持续一段时间的N2和O2,以保证氮的氧化物被充分吸收。计算参加反应的硝酸的物质的量可以利用原子守恒进行计算,反应后剩余硝酸是0.04mol,反应前硝酸是0.04L×13.5mol/L=0.54mol,剩余参加反应的硝酸是0.5mol。因为溶液中含有银离子,剩余可以通过沉淀法来测定银的物质的量。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com