
题目列表(包括答案和解析)
【10分】某学生用胆矾制取氧化铜固体,并研究氧化铜能否在氯酸钾受热分解实验中起催化作用。实验步骤如下:
①称量a g胆矾固体放入烧杯中,加水制成溶液,向其中滴加氢氧化钠溶液至沉淀完全;
②把步骤①中的溶液和沉淀转移至蒸发皿中,加热至溶液中的沉淀全部变成黑色氧化铜为止;
③过滤、洗涤、干燥,称量所得固体质量为b g;
④取一定质量的上述氧化铜固体和一定质量的氯酸钾固体,混合均匀后加热,收集反应生成的氧气,如下图所示。
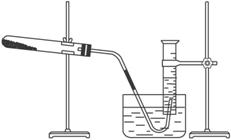
请回答下列问题。
(1)上述各步操作中,需要用到玻璃棒的是_________ (填写前面所述实验步骤的序号)。
(2)由胆矾制备氧化铜的产率(实际产量与理论产量的百分比)为_________×100%。
(3)为保证Cu2+沉淀完全,步骤①中溶液的pH应大于10。简述用pH试纸测定溶液pH的操作:____________________________________________________________________。
(4)为证明氧化铜在氯酸钾的分解反应中起催化作用,在上述实验①—④后还应该进行的实验操作是(按实验先后顺序填写字母序号) _________。
a.过滤 b.烘干 c.溶解 d.洗涤 e.称量
(5)但有的同学认为,还必须另外再设计一个实验才能证明氧化铜在氯酸钾受热分解的实验中起催化作用。你认为还应该进行的另一个实验是_________________________________。
(每空格3分,计15分)某研究小组在实验室探究氨基甲酸铵(NH2COONH4)分解反应平衡常数和水解反应速率的测定。
将一定量纯净的氨基甲酸铵置于特制的密闭真空容器中(假设容器体积不变,固体试样体积忽略不计),在恒定温度下使其达到分解平衡:NH2COONH4(s) 2NH3(g)+CO2(g)。
2NH3(g)+CO2(g)。
实验测得不同温度下的平衡数据列于下表:
| 温度(℃) | 15.0 | 20.0 | 25.0 | 30.0 | 35.0 |
| 平衡总压强(kPa) | 5.7 | 8.3 | 12.0 | 17.1 | 24.0 |
| 平衡气体总浓度 (×10-3mol/L) | 2.4 | 3.4 | 4.8 | 6.8 | 9.4 |
 B.密闭容器中总压强不变
B.密闭容器中总压强不变| ①镁、铝、锌都是银白色的金属 ②锌(Zn)可以与NaOH溶液反应生成H2 ③Zn(OH)2为白色固体,难溶于水,可溶于强碱及NH3?H2O ④Zn2+易形成络合物如[Zn(NH3)4]2+,该络合物遇强酸转化变成Zn2+、NH4+●提出假设: (1)假设①:该混合金属粉末中除镁外还含有 假设②:该混合金属粉末中除镁外还含有 假设③:该混合金属粉末中除镁外还含有铝、锌. ●实验探究: 甲同学基于假设③设计实验方案: 操作Ⅰ是在滤液中逐滴加入稀硫酸,直至生成的沉淀刚好溶解,再加足量的稀氨水,请回答:  乙同学基于假设③设计另一方案:  (2)沉淀A、B、D的化学式:A (3)甲同学用样品和稀硫酸反应所得溶液含有较多H+、Mg2+、Al3+、SO42-,向其中滴入NaOH溶液,生成沉淀的量与加入NaOH溶液体积关系可能正确的是  (4)乙同学方案的操作②中,铝与NaOH溶液反应的化学方程式为 操作②与操作③中都加了NaOH溶液,但其用量差别是 (5)丙同学通过分析对比,认为乙的方案比甲同学的好,其理由可能是 (2011?云浮模拟)某混合金属粉末,除Mg外,还含有Al、Zn中的一种或两种,含量都在10%以上.某研究小组设计实验探究该混合金属粉末中铝、锌元素的存在.所用试剂:样品、pH试纸、稀H2SO4、NaOH溶液、稀NH3?H2O.该小组探究过程如下: ●查阅资料:
|