利用焦炭或天然气制取廉价的CO和H
2,再用于氨合成和有机合成是目前工业生产的重要途径.
(1)已知:CH
4(g)+2O
2 (g)=CO
2 (g)+2H
2O (l)△H=-890.3kJ?mol
-1 ①
H
2(g)+1/2O
2 (g)=H
2O (l)△H=-285.8kJ?mol
-1 ②
CO(g)+1/2O
2(g)=CO
2(g)△H=-283.0kJ?mol
-1 ③
H
2O(g)=H
2O(l)△H=-44.0kJ?mol
-1 ④
反应CH
4(g)+H
2O(g)
CO(g)+3H
2(g),△H=______kJ?mol
-1.标准状况下33.6L甲烷高温下与水蒸气完全反应生成CO和H
2,反应过程中转移______mole
-,放出______kJ热量.
(2)一定条件下,在体积为5L的密闭容器中,一氧化碳与氢气反应生成甲醇(催化剂为Cu
2O/ZnO):CO(g)+2H
2(g)?CH
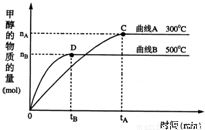
3OH(g).不同温度时甲烷的物质的量随时间变化曲线如图所示.根据题意完成下列各题:
①反应达到平衡时,平衡常数表达式K=______,降低温度,K值______(填“增大”、“减小”或“不变”).
②在300℃,从反应开始到平衡,氢气的平均反应速率v(H
2)=______.(用相关符号和数据表示)
③判断该可逆反应达到平衡状态的标志是______.(填字母)
a.CH
3OH的生成速率与CO的消耗速率相等 b.容器中气体的压强不变
c.容器中混合气体的密度保持不变 d.CO百分含量保持不变
e.CO和CH
3OH浓度相等
④欲提高H
2的转化率,下列措施可行的是______.(填字母)
a.向容器中再充入Ar b.改变反应的催化剂
c.向容器中再充入CO d.升高温度.

 利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径.
利用焦炭或天然气制取廉价的CO和H2,再用于氨合成和有机合成是目前工业生产的重要途径.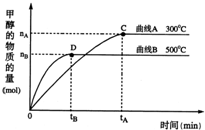
 CO(g)+3H2(g),△H= kJ?mol-1.标准状况下33.6L甲烷高温下与水蒸气完全反应生成CO和H2,反应过程中转移 mole-,放出 kJ热量.
CO(g)+3H2(g),△H= kJ?mol-1.标准状况下33.6L甲烷高温下与水蒸气完全反应生成CO和H2,反应过程中转移 mole-,放出 kJ热量.