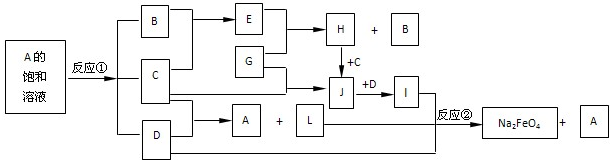
下图中的反应①是重要的电化学工业反应,反应②可用于制备新型消毒净水剂Na
2FeO
4.常温下B、C为气态单质,G是当代社会使用量最大的金属,其余均为化合物.(反应时加入或生成的水,以及生成沉淀I时的其他产物均已略去).

请回答下列问题:
(1)E的电子式为
.
(2)J溶液蒸干灼烧得到的物质是(填化学式)
Fe2O3
Fe2O3
.
(3)反应①的化学方程式是
.
(4)反应②的离子方程式是
2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O
2Fe(OH)3+3ClO-+4OH-=2FeO42-+3Cl-+5H2O
.
(5)高铁酸钠(Na
2FeO
4)是一种新型、高效、无二次污染的绿色水处理剂.工业上干法制备高铁酸钠的主要反应方程式为:FeSO
4+Na
2O
2→Na
2FeO
4+Na
2O+Na
2SO
4+O
2↑(未配平)
下列有关说法不正确的是
BD
BD
A.高铁酸钠中铁显+6价
B.干法中每生成1mol Na
2FeO
4转移4mol电子
C.Na
2FeO
4处理水时,不仅能消毒杀菌,还能除去水体中的H
2S、NH
3等
D.Na
2FeO
4处理水时还能吸附水中的悬浮杂质,所以自来水厂用高铁酸钠处理水后无需再用活性炭处理了.