
题目列表(包括答案和解析)
|
已知热化学方程2KNO3(s)=2KNO2(s)+O2(g);△H=+58kJ/mol;C(s)+O2(g)=CO2(g);△H=-94kJ/mol.为提供分解1molKNO3所需能量理论上需燃烧碳 | |
| [ ] | |
A. |
58/94mol |
B. |
58/(94×2)mol |
C. |
(58×2)/94mol |
D. |
(94×2)/58mol |
(15分)X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
|
元素 |
相关信息 |
|
X |
X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
|
Y |
常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
|
Z |
Z和Y同周期,Z的电负性大于Y |
|
W |
W的一种核素的质量数为63,中子数为34 |
(1)Y元素位于周期表中 区,该元素原子核外共有 种不同运动状态的电子。
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键,该分子中中心原子的杂化类型为 。在H―Y、H―Z两种共价键中,键的极性较强的是 ,键长较长的是 。
(3)W的基态原子外围电子排布式是 。
(4)请写出元素W的单质与元素Y的最高价氧化物对应水化物的浓溶液在一定条件下发生反应的化学方程 。
(5)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:
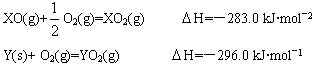
此反应的热化学方程式是 。
(15分)X、Y、Z、W是元素周期表前四周期中的四种常见元素,其相关信息如下表:
| 元素 | 相关信息 |
| X | X的基态原子核外3个能级上有电子,且每个能级上的电子数相等 |
| Y | 常温常压下,Y单质是淡黄色固体,常在火山口附近沉积 |
| Z | Z和Y同周期,Z的电负性大于Y |
| W | W的一种核素的质量数为63,中子数为34 |
(1)Y元素位于周期表中 区,该元素原子核外共有 种不同运动状态的电子。
(2)XY2是一种常用的溶剂,XY2的分子中存在 个σ键,该分子中中心原子的杂化类型为 。在H―Y、H―Z两种共价键中,键的极性较强的是 ,键长较长的是 。
(3)W的基态原子外围电子排布式是 。
(4)请写出元素W的单质与元素Y的最高价氧化物对应水化物的浓溶液在一定条件下发生反应的化学方程 。
(5)处理含XO、YO2烟道气污染的一种方法,是将其在催化剂作用下转化为单质Y。
已知:
此反应的热化学方程式是 。
2007年度http://today.ks5u.com诺贝尔化学奖获得者格哈德·埃特尔建立了合成氨反应机理,T=673K时,各步反应的能量变化如图所示,图中的能量单位为kJ·mol-1。(注:图中“吸”表示在催化剂表面的吸附)请回答下列问题:
(1)合成氨反应的机理为
① ;
![]()
![]()
![]() ②N2 N2吸 2N 2N吸
②N2 N2吸 2N 2N吸
③ ;
![]() ④NH吸+H吸 NH2吸;
④NH吸+H吸 NH2吸;
![]()
![]() ⑤NH2吸+H吸 NH3吸 NH3。
⑤NH2吸+H吸 NH3吸 NH3。
(2)T=673K时,合成氨反应的热化学方程为 。
(3)液氨与水颇为相像,它能溶解多种无机及有机分子,其电离方程式可表示为:
![]() 2NH3 NH+4+NH-2(某温度http://today.ks5u.com下其离子积常数为10-30)。液氨中的pNH4与水中的pH类似,则该温度http://today.ks5u.com下液氨的pNH4= 。
2NH3 NH+4+NH-2(某温度http://today.ks5u.com下其离子积常数为10-30)。液氨中的pNH4与水中的pH类似,则该温度http://today.ks5u.com下液氨的pNH4= 。
(4)盐酸肼(N2H4Cl2)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与NH4Cl类似。写出盐酸肼第一步水解反应的离子方程式 。
(5)肼(N2H4)又称联氨,是一种可燃性的液体,可用作火箭燃料。已知在101kPa时,N2H4在氧气中完全燃烧生成氮气,肼—空气燃料电池是一种碱性燃料电池,电解质溶液是20%~30%的KOH溶液。肼—空气燃料电池放电时:
负极的电极反应式是 。
(1)在101 kPa时,CO在1.0 mol O2中完全燃烧,生成2.0 mol CO2,放出566.0 kJ的热量, 则此反应的热化学方程: ;
又已知:2H2(g)+O2(g)=2H2O(g);ΔH=-483.6 kJ/mol,请写出CO2与H2反应生成CO和水蒸气的热化学方程: 。
(2) 拆开1molH-H键、1molN-H键、1molN≡N键分别需要能量是436KJ、391KJ、946KJ,若有1mol N2与H2恰好完全反应生成NH3,则反应的ΔH= 。
(3) 某温度时,在2 L容器中X、Y、Z三种物质的量随 时间的变化曲线如右图所示。由图中数据分析,该反应的化学方程式为: 。
(4) 一定温度下的密闭容器中存在如下反应:
2SO2(g)+O2(g) ![]() 2SO3(g),已知c始(SO2)=0.4mol·L-1,c始(O2)=1mol·L-1,经测定该反应在该温度下的平衡常数K=19,试判断:
2SO3(g),已知c始(SO2)=0.4mol·L-1,c始(O2)=1mol·L-1,经测定该反应在该温度下的平衡常数K=19,试判断:
当SO2转化率为50%时,该反应 (填“是”或“否”)达到平衡状态,若未达到,则向 (填“正”或“逆”, 若已达到平衡此空可不填)方向进行。

湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com