
题目列表(包括答案和解析)
中和滴定是利用已知物质的量浓度的酸(或碱)来测定未知物质的量浓度的碱(或酸),
若用A代表酸,用B代表碱,可以利用下式来计算未知碱的物质的量浓度的是(ν为化学计量数)
A.cB=![]() B.cB=
B.cB=![]() C.cB=
C.cB=![]() D.cB=
D.cB=![]()
A.cB=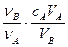 | B.cB=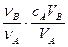 | C.cB=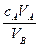 | D.cB=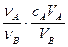 |




(12分)中和滴定实验:
⑴ 取体积相同(25mL)的两份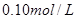
 溶液,将其中一份放在空气中一段时间后,溶液的pH
(填“增大”“减小”或“不变”)。用已知浓度的盐酸中和上述两份溶液。若中和放在空气中一段时间后的那份溶液消耗盐酸的体积为
溶液,将其中一份放在空气中一段时间后,溶液的pH
(填“增大”“减小”或“不变”)。用已知浓度的盐酸中和上述两份溶液。若中和放在空气中一段时间后的那份溶液消耗盐酸的体积为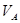 ,中和另一份溶液消耗盐酸的体积为
,中和另一份溶液消耗盐酸的体积为 ,则①以甲基橙为指示剂
,则①以甲基橙为指示剂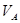 和
和 的关系是
。②以酚酞为指示剂时,
的关系是
。②以酚酞为指示剂时,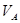 和
和 的关系是
。
的关系是
。
⑵ 某烧碱样品含少量不与酸作用的杂质,为了测定其纯度,进行以下滴定操作
A. 在250mL的容量瓶中定容配成250mL烧碱溶液
B. 用移液管移取25mL烧碱溶液于锥形瓶中并滴几滴指示剂甲基橙
C. 在天平上准确称取烧碱样品Wg,在烧杯中用蒸馏水溶解
D. 将物质的量浓度为C的标准硫酸溶液装入酸式滴定管,调节液面,
记下开始读数为V1
E. 在锥形瓶下垫一张白纸,滴定至终点,记下读数V2
回答下列各问题:
①正确操作步骤的顺序是(用字母填写) → → → D → 。
②滴定前或滴定后读数时应注意 。
③E中在锥形瓶下垫一张白纸的作用是 。
④D步骤中液面应调节到 ,尖嘴部分应 。[来源:学。科。网Z。X。X。K]
⑤滴定终点时颜色变化是 。
⑥若酸式滴定管不用标准硫酸润洗,在其它操作均正确的前提下,会使测定结果
(指烧碱的纯度) (指偏高、低或不变)
⑦该烧碱样品纯度的计算式为 。
酸碱中和反应是中学化学一类重要的反应,其反应的本质都是H+和OH-反应生成H2O.某学生实验小组对课本中的两个酸碱中和实验进行了模拟研究.
(1)用下图装置进行强酸(50 mL 0.5 mol/L的HCI)和强碱(50 mL 0.55 mol/L的NaOH)反应的中和热测定.
①从实验装置上看,图中尚缺少的一种玻璃仪器是________;
②大小烧杯之间填满纸屑的作用是________;
③向组装好的量热器中加入50 mL盐酸并测定温度,取出温度计并冲
净后,再将已测定好温度的NaOH溶液50 mL加入量热器.下列加入50 mL NaOH溶液的操作正确的是________.
A.为了使酸碱充分中和,必须边滴加NaOH溶液边迅速搅拌
B.把50 mL NaOH溶液一次迅速倒入,盖上纸板迅速搅拌.
④若用醋酸代替上述盐酸实验,实验测得的中和热值________(填偏大、偏小或无影响).
(1)、用实验室准确配制的0.100 mol/L的NaOH溶液测定某未知浓度的稀盐酸.
其具体实验步骤如下:
①取一支碱式滴定管下图中有两只滴定管~上端未画出,你选择哪一只?________(填写对应字母),用少量标准NaOH溶液润洗2~3次水洗后的碱式滴定管,再加入标准的0.100 mol/L的NaOH溶液并记录液面刻度读数;
②用酸式滴定管精确的放出25.00 mL待测盐酸,置于用蒸馏水洗净的锥形瓶中,再加入酚酞(变色范围:8.2~10.0)试液2滴;
③滴定时,边滴边振荡,同进注视眼睛注视锥形瓶内容也颜色的变化,当锥形瓶内溶液由________(填写颜色变化)且半分钟内不褪色时,即达到滴定终点;
④记录液面刻度读数.根据滴定管的两次读数得出消耗标准盐酸的体积,再重复测定两次,实验结果记录见下表:

测得未知稀盐酸的物质的量浓度为________(保留小数点后3位).
⑤如果滴定结束时俯视碱式滴定管刻度读数(其它操作均正确),则对滴定结果~稀盐酸浓度的影响是________(填“偏高”、“偏低”或“无影响”).
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com