
题目列表(包括答案和解析)
(10分)工业制硫酸生产流程如下图:

(1)在气体进入催化反应室前,需净化的原因是:________________________________。
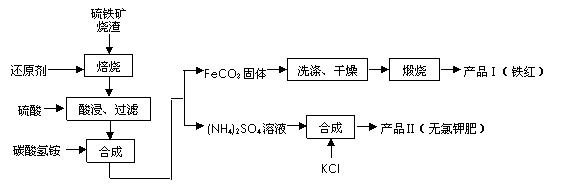
(2)在制气过程中,我国往往以黄铁矿为原料制SO2 ,其铁矿烧渣(主要成分为Fe2O3、Fe3O4、FeO、SiO2等)是生产硫酸的工业废渣,综合利用对环境保护具有现实意义。利用硫铁矿烧渣制备铁红等产品的实验流程如下:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
![]()
已知几种盐的溶解度随温度变化的曲线如下图所示:
![]()
![]()
![]()
![]()
![]()
![]()
![]()
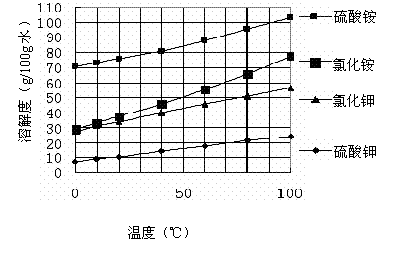
则:
①酸浸、过滤后滤液中的金属阳离子是________________。
②煅烧FeCO3生成产品Ⅰ的化学反应方程式为_______________________________ _。
③产品Ⅱ的化学式为_______________
④检验产品II中是否含有氯化物杂质的实验操作是:取少量产品Ⅱ于试管中配成溶液,
(分)有A、B、C、D四种元素,A元素形成的离子中只有一个质子,B原子的最外层电子数是次外层的3倍,C元素的一价阳离子核外有10个电子,D元素的原子得到一个电子后能形成与氩原子电子层结构相同的离子。回答下列列问题:
(1)画出D元素的离子结构示意图__________________;
(2)工业上用电解C和D两元素形成的化合物的水溶液生产D的单质,写出该反应的化学方程式_______________________,电解后的溶液能使酚酞变红的是与电源的________极相连接的区域;
(3)D单质能和A、B、C三元素形成的化合物反应,该反应的化学方程式是________________,当有0.1mol的D单质反应时,电子转移__________个;
(4)B、C、D三元素能形成一种化合物,1mol该化合物中有36mol电子,该化合物的水溶液是一种____剂,它与A、D两元素形成的化合物的水溶液反应时能产生一种有毒气体,该反应的化学方程式是______。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com