
题目列表(包括答案和解析)
(2005·江苏)在一定条件下,烯烃可发生臭氧化还原水解反应,生成羰基化合物,该反应可表示为:
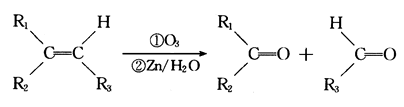
已知:
①化合物A,其分子式为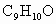 ,它既能使溴的四氯化碳溶液褪色,又能与
,它既能使溴的四氯化碳溶液褪色,又能与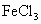 溶液发生显色反应,且能与金属钠或NaOH溶液反应生成B.
溶液发生显色反应,且能与金属钠或NaOH溶液反应生成B.
②B发生臭氧化还原水解反应生成C,C能发生银镜反应.
③C催化加氢生成D,D在浓硫酸存在下加热生成E.
④E既能使溴的四氯化碳溶液褪色,又能与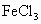 溶液发生显色反应,且能与NaOH溶液反应生成F.
溶液发生显色反应,且能与NaOH溶液反应生成F.
⑤F发生臭氧化还原水解反应生成G,G能发生银镜反应,遇酸转化为 .
.
请根据上述信息,完成下列填空:
(1)写出下列化合物的结构简式(如有多组化合物符合题意,只要求写出其中的一组):
A________,C________,E________.
(2)写出分子式为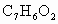 的含有苯环的所有同分异构体的结构简式________.
的含有苯环的所有同分异构体的结构简式________.
实验化学:
2005年江苏酸雨污染有所加重,酸雨发生频率为34.1%,上升了6.2个百分点,每三场雨中就有一场多是酸雨.某校研究性学习小组拟对本市空气中二氧化硫含量(mg·m-3)进行测定.经查阅资料可用以下方法测定:
实验原理:大气中的二氧化硫用甲醛溶液吸收后,生成稳定的羟甲基磺酸加成化合物,再加入氢氧化钠使加成化合物分解,释放出二氧化硫与副玫瑰苯胺、甲醛作用,生成紫红色化合物.据其颜色深浅,用分光光度计在577 nm处进行测定.
分光光度计是利用分光光度法对物质进行定量定性分析的仪器.而分光光度法则是通过测定被测物质在特定波长时光的吸收度,对该物质进行定性和定量分析.其工作原理可以简单的用公式表示为A=KC,其中A为吸光度,K为一定条件下的常数,C为溶液浓度.
实验步骤:(1)采样:
①如果你是该兴趣小组成员,你对采样的地点和时间有何建议:
___________________________________
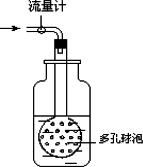
②用如图装置采样,通过50 L空气后,将吸收液移入100 ml容量瓶,用少量吸收液分两次洗涤吸收装置,合并洗涤液于容量瓶中,定容备用.
用多孔球泡而不用导管的原因是____________________________.
(2)吸光度与SO2含量标准曲线的绘制:在6支25 ml比色管中,用每毫升含25 μg二氧化硫的标准液配置下表标准SO2含量系列.
二氧化硫标准系列

用10 mL比色皿,以水为参比,测定各管吸光度,实验结果如下.

以吸光度值为纵坐标,二氧化硫含量(μg/10 mL)为横坐标,绘制标准曲线
(3)准确量取容量瓶中溶液10 mL加入比色皿,测得其吸光度值为0.10,则空气中二氧化硫含量为________mg·m-3.我国环境空气质量标准中对每次空气质量测定中SO2的最高浓度限值(mg/m3):一级标准:0.15二级标准:0.50三级标准:0.70.则该市空气为________级标准.
(4)甲、乙两组同学测定结果相差较大,乙组同学测定空气中SO2含量偏小,试分析乙组同学出现误差的可能原因:(两个所用药品和装置均无问题)
_______________________________________
(5)请你提出江苏防治酸雨的两条主要措施:
_______________________________________
2005年江苏酸雨污染有所加重,酸雨发生频率为34.1%,上升了6.2个百分点,每三场雨中就有一场多是酸雨。某校研究性学习小组拟对本市空气中二氧化硫含量(![]() )进行测定。经查阅资料可采用以下方法:
)进行测定。经查阅资料可采用以下方法:
实验原理:大气中的二氧化硫用甲醛溶液吸收后,生成稳定的羟甲基磺酸加成化合物,再加入氢氧化钠使加成化合物分解,释放出二氧化硫,与副玫瑰苯胺、甲醛作用,生成紫红色化合物。据其颜色深浅,用分光光度计在577nm处进行测定。
分光光度计是利用分光光度法对物质进行定量、定性分析的仪器。而分光光度法则是通过测定被测物质在特定波长时光的吸收度,对该物质进行定性和定量分析。其工作原理可以简单地用公式表示为![]() ,其中A为吸光度,K为一定条件下的常数,c为溶液浓度。
,其中A为吸光度,K为一定条件下的常数,c为溶液浓度。

实验步骤:
(1)采样:
①若你是该兴趣小组成员,你对采样的地点和时间有何建议:
②用图装置采样。通过50L空气后,将吸收液移入100mL容量瓶,用少量吸收液分两次洗涤吸收装置,合并洗涤液于容量瓶中,定容备用。用多孔球泡而不用导管的原因是
(2)吸光度与![]() 含量标准曲线的绘制:在6支25mL比色管中,用每毫升含25
含量标准曲线的绘制:在6支25mL比色管中,用每毫升含25![]() 二氧化硫的标准液配置下表中的标准
二氧化硫的标准液配置下表中的标准![]() 含量系列。
含量系列。
二氧化硫标准系列
| 管号 | 0 | 1 | 2 | 3 | 4 | b |
| 标准液/mL | 0 | 0.20 | 0.40 | 0.60 | 0.80 | 1.00 |
| 吸收液/mL | 10.00 | 9.80 | 9.60 | 9.40 | 9.20 | 9.00 |
| 二氧化硫含量/ | 0 | 5.00 | 10.00 | 15.00 | 20.00 | 25.00 |
用10mL比色皿,以水为参比,测定各管吸光度,实验结果如下。
| 管 号 | 0 | 1 | 2 | 3 | 4 | 5 |
| 吸光度 | 0 | 0.20 | 0.40 | 0.60 | 0.80 | 1.00 |
以吸光度值为纵坐标,二氧化硫含量(![]() )为横坐标,绘制标准曲线。
)为横坐标,绘制标准曲线。
(3)准确量取容量瓶中溶液10mL加人比色皿,测得其吸光度值为0.24,则空气中二氧化硫含量为 ![]() 。我国环境空气质量标准中对每次空气质量测定中
。我国环境空气质量标准中对每次空气质量测定中![]() 的最高浓度限值(m9/m3):一级标准:0.15,二级标准:0.50,三级标准:0.70。则该市空气为 级标准。
的最高浓度限值(m9/m3):一级标准:0.15,二级标准:0.50,三级标准:0.70。则该市空气为 级标准。
(4)甲、乙两组同学测定结果相差较大,试分析乙组同学测定空气中![]() 含量偏小的可能原因:(两个所用药品和装置均无问题)
含量偏小的可能原因:(两个所用药品和装置均无问题)
(5)请你提出江苏防治酸雨的两条主要措施:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com