
题目列表(包括答案和解析)
A.在t1时间内用B表示该反应的平均速率为0.6 mol·L-1·min-1
B.在t1+10时,保持其他条件不变,增大压强,平衡向逆反应方向移动
C.T ℃时,在相同容器中,若由0.1 mol·L-1 A、0.3 mol·L-1 B和0.4 mol·L-1 C反应,达到平衡后,C的浓度仍为0.4 mol·L-1
D.在其他条件不变时,升高温度,正、逆反应速率均增大,且A的转化率增大
|
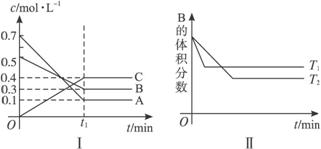
T℃时,反应物和生成物均为气体的某反应,反应过程中浓度变化如下图(Ⅰ)所示.若保持其他条件不变,温度分别为T1和T2时,B的体积分数与时间的关系如下图(Ⅱ)所示,则下列结论正确的是
| |
| [ ] | |
A. |
在t1时间内用B表示该反应的平均速率为:0.6 mol·L-1·min-1 |
B. |
在(t1+10)时,保持其他条件不变,增大压强,平衡向逆反应方向移动 |
C. |
T℃时,在相同容器中,若由0.1 mol·L-1 A、0.3 mol·L-1 B和0.4 mol·L-1 C反应,达到平衡后,C的浓度仍为0.4 mol·L-1 |
D. |
在其他条件不变时,升高温度,正、逆反应速率均增大,且A的转化率增大 |

 2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是______.
2SO3△H<0,下图表示该反应的速率(v)随时间(t)变化的关系,t2、t3、t5时刻外界条件有所改变,但都没有改变各物质的初始加入量.下列说法中正确的是______. 2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m.
2SO3达到平衡后,SO3的体积分数为 a%,SO2的转化率为m. ![]()
(1)若A 是一种溶液,其溶质由三种不同短周期元素构成,这三种元素中有两种处于同一主族,且三种元素原子的最外层电子数之和为8,则X的化学式可能为____________、____________(填两种不同类别的物质);若此时X为一种18电子的分子, 则C的化学式为____________,在B的溶液中加入新制的AgCl悬浊液,白色浑浊立即变成黑色浑浊,由此现象可以得出的结论是____________________________________。
(2)若A是一种10电子分子,B在通常情况下遇X即生成C,又知
(3)若A是一种黄色的固体非金属单质,则反应②的化学方程式是_________________。
某温度T时,在一定条件下的
①物质B的转化率____________________________________。
②该温度下反应②的平衡常数____________________________________。
③在上述相同的条件下,向相同的容器中投入2 mol C,请在右下图中画出从反应开始至t2时间达到平衡后各物质的物质的量与时间的关系图。

下图是煤化工产业链的一部分,试运用所学知识,解决下列问题: 
I.已知该产业链中某反应的平衡表常数达式为:K= ,它所对应反应的化学方程式为 。
,它所对应反应的化学方程式为 。
II.二甲醚(CH3OCH3)在未来可能替代柴油和液化气作为洁净液体燃料使用,工业上以CO和H2为原料生产CH3OCH3。工业制备二甲醚在催化反应室中(压力2.0~10.0Mpa,温度230~280℃)进行下列反应:
①CO(g)+2H2(g) CH3OH(g) △H1=-90.7kJ·mol-1
CH3OH(g) △H1=-90.7kJ·mol-1
②2CH3OH(g) CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
CH3OCH3(g)+H2O(g) △H2=-23.5kJ·mol-1
③CO(g)+H2O(g) CO2(g)+H2(g) △H3=-41.2kJ·mol-1
CO2(g)+H2(g) △H3=-41.2kJ·mol-1
(1)催化反应室中总反应的热化学方程式为 。
830℃时反应③的K=1.0,则在催化反应室中反应③的K 1.0(填“>”、“<”或“=”)。
(2)在某温度下,若反应①的起始浓度分别为:c(CO)=1 mol/L,c(H2)=2.4 mol/L,5 min后达到平衡,CO的转化率为50%,则5 min内CO的平均反应速率为 ;若反应物的起始浓度分别为:c(CO)=4 mol/L,c(H2)=a mol/L;达到平衡后,c(CH3OH)=2 mol/L,a= mol/L。
(3)反应②在t℃时的平衡常数为400,此温度下,在0.5L的密闭容器中加入一定的甲醇,反应到某时刻测得各组分的物质的量浓度如下:
| 物质 | CH3OH | CH3OCH3 | H2O |
| c(mol/L) | 0.8 | 1.24 | 1.24 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com