
题目列表(包括答案和解析)
I.(8分)A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有5个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A的最高价氧化物的水化物是___________(填化学式);
(2)物质E中所包含的化学键有______________,写出C、D两元素形成的化合物C2D的电子式______________________;
(3)把盛有48 mL AB、AB2混合气体的容器倒置于水中(同温、同压下),待液面稳定后,容器内气体体积变为24 mL,则原混合气体中AB的体积分数为__________。
II.(6分)下表为长式周期表的一部分,其中的编号代表对应的元素。
请回答下列问题:
(1)写出元素⑩的基态原子的电子排布式_________________。
(2)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子数为_____
(3)③④⑤三种元素的第一电离能由大到小的顺序是(填序号)___________。
I.(8分)A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有5个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A的最高价氧化物的水化物是___________(填化学式);
(2)物质E中所包含的化学键有______________,写出C、D两元素形成的化合物C2D的电子式______________________;
(3)把盛有48 mL AB、AB2混合气体的容器倒置于水中(同温、同压下),待液面稳定后,容器内气体体积变为24 mL,则原混合气体中AB的体积分数为__________。
II.(6分)下表为长式周期表的一部分,其中的编号代表对应的元素。

请回答下列问题:
(1)写出元素⑩的基态原子的电子排布式_________________。
(2)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子数为_____
(3)③④⑤三种元素的第一电离能由大到小的顺序是(填序号)___________。
I.(8分)A、B、C、D四种短周期元素,原子序数依次增大,A原子的最外层上有5个电子;B的阴离子和C的阳离子具有相同的电子层结构,两元素的单质反应,生成一种淡黄色的固体E,D的L层电子数等于K、M两个电子层上的电子数之和。
(1)A的最高价氧化物的水化物是___________(填化学式);
(2)物质E中所包含的化学键有______________,写出C、D两元素形成的化合物C2D的电子式______________________;
(3)把盛有48 mL AB、AB2混合气体的容器倒置于水中(同温、同压下),待液面稳定后,容器内气体体积变为24 mL,则原混合气体中AB的体积分数为__________。
II.(6分)下表为长式周期表的一部分,其中的编号代表对应的元素。
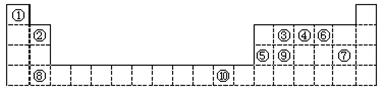
请回答下列问题:
(1)写出元素⑩的基态原子的电子排布式_________________。
(2)某元素的特征电子排布式为nsnnpn+1,该元素原子的核外最外层电子的成对电子数为_____
(3)③④⑤三种元素的第一电离能由大到小的顺序是(填序号)___________。
(共13分)A、B、C、D、E、F、G、L、I九种主族元素分布在三个不同的短周期,它们的原子序数依次增大,其中B、C、D为同一周期,A与E、B与G、D与L分别为同一主族,C、D、F三种元素的原子序数之和为28,F的质子数比D多5,D的最外层电子数是F的2倍,C和D的最外层电子数之和为11。请回答下列问题:
(1)以上八种元素中非金属所形成的最简单气态氢化物稳定性最弱的是(填化学式)____________,E、F、L所形成的简单离子的半径由大到小的顺序为(用离子符号表示)__ __ > > 。
(2)由L、I两元素可按原子个数比1:1组成化合物X,化合物X中各原子均满足8电子的稳定结构,则X的电子式为 。固体化合物E2D2投入到化合物E2L的水溶液中,只观察到有沉淀产生的,写出该反应的离子方程式为: 。
(3)在10 L的密闭容器中,通入2mol LD2气体和1 mol D2气体,一定温度下反应后生成LD3气体,当反应达到平衡时,D2的浓度为0.01 mol·L-1,同时放出约177 kJ的热量,则平衡时LD2的转化率为 ;该反应的热化学方程式为 ;此时该反应的平衡常数K= 。
(4) 有人设想寻求合适的催化剂和电极材料,以C2、A2为电极反应物,以HCl—NH4Cl溶液为电解质溶液制造新型燃料电池,试写出该电池的正极反应式 ;
【8分】下图是部分短周期元素的单质及其化合物的转化关系图(有关反应条件及生成的水已略去),已知:A、B、C、D为四种非金属单质,其中B、C、D在常温常压下是气体;反应①②是化工生产中的重要反应;化合物E是形成酸雨的污染物之一,化合物K是常用的氮肥,化合物L具有漂白性,可由Cl2与NaOH反应而制得,J由两种元素组成,其相对分子质量为32。按要求填空:

(1)A元素在周期表中的位置是______________;
(2)J的化学式为______________;
(3)写出L溶液与化合物E反应的离子方程式:________________________________;
(4)将F水溶液与盐酸混合得到一种无色透明溶液,在此溶液中只含有四种离子,按四种离子浓度从大到小顺序把它们可能的一种关系表示出来。
| 溶液酸碱性 | 离子浓度大小顺序 | |
| 1 | 酸性 | |
| 2 | 中性 | |
| 3 | 碱性 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com