图1是化学研究性学习小组设计的铜与稀硝酸反应的两个实验装置图.其中装置Ⅰ为甲同学设计.(可能用到的相对原子质量:H:1 C:12 N:14 O:16 Cu:64 )
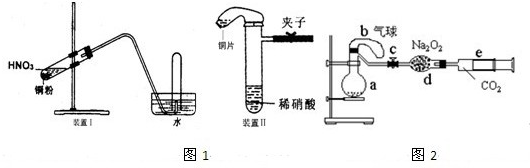
请回答下列问题:
(1)铜与稀硝酸反应的离子方程式为
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
3Cu+8H++2NO3-=3Cu2++2NO↑+4H2O
.
(2)乙同学认为装置Ⅰ中收集的气体不能确定铜与稀硝酸反应生成的是NO气体,理由是
NO2与水反应也可产生NO:3NO2+H2O=2HNO3+NO,故不能肯定生成的NO气体是来自于铜与稀硝酸反应
NO2与水反应也可产生NO:3NO2+H2O=2HNO3+NO,故不能肯定生成的NO气体是来自于铜与稀硝酸反应
.于是他设计装置Ⅱ,其中装铜片的是气球.
(3)化学研究性学习小组的其它同学对上述实验进行了研究,认为装置Ⅱ只能定性研究铜与硝酸的反应,他们又重新设计了一套实验,装置图如图2:a中盛有标况下的空气(氧气占五分之一)和10mL,1.2mol/L硝酸的250mL烧瓶.b是未充气(实验开始前内部没有气体)放有0.384g铜粉的气球.(整套装置已经过气密性检查合格.)他们做了以下实验,请填写有关空白:
①将气球中的铜粉小心倒入烧瓶中,充分反应后发现 铜粉有余(设产生的气体不溶解于溶液中),则可观察到的是
溶液变蓝色,烧瓶内气体由无色继而变成红色,气球胀大
溶液变蓝色,烧瓶内气体由无色继而变成红色,气球胀大
;
②将烧瓶不断振荡发现气球逐渐缩小,发生有关反应的化学方程式是:
NO2+O2+2H2O═4HNO3、或4NO+3O2+2H2O═4HNO3
NO2+O2+2H2O═4HNO3、或4NO+3O2+2H2O═4HNO3
;
③打开弹簧夹将二氧化碳慢慢推入干燥管内继续振荡,使气体与气体、溶液充分接触,欲使所有的铜粉都溶解,至少需要推入二氧化碳
38.4
38.4
ml;
④将上述全过程用一个总的化学方程式表示:
2Cu+4HNO3+O2═2Cu(NO3)2+2H2O
2Cu+4HNO3+O2═2Cu(NO3)2+2H2O
.

![]() )、c(HCO3¯)都减少,其方法是( )
)、c(HCO3¯)都减少,其方法是( )![]() )、c(HCO3¯)都减少,其方法是( )
)、c(HCO3¯)都减少,其方法是( )