
题目列表(包括答案和解析)
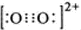
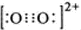
A、B、C、D、E是周期表中前四周期的元素,其有关性质或结构信息如下表:
元素 有关性质或结构信息
A 负二价的A元素的氢化物在通常状况下是一种液体,其中A的质量分数为88.9%
B B原子得到一个电子后3p轨道全充满
C C原子的p轨道半充满,它的气态氢化物能与其最高价氧化物的水化物反应生成一种常见的盐X
D D元素的最高化合价与最低化合价的代数和为零,其最高价氧化物为分子晶体
E E元素的核电荷数等于A原子和B元素氢化物的核电荷数之和
(1)元素Y是C下一周期同主族元素,比较B、Y元素的第一电离能I1(B) I1(Y)。
(2)E元素原子的核外电子排布式为
(3)盐X的水溶液呈 (填“酸性”、“碱性”或“中性”),B元素最高价含氧酸一定比D元素最高价含氧酸的酸性 (填“强”或“弱”)。
(4)C单质分子中σ键和π键的个数比为 ,C的氢化物在同族元素的氢化物中沸点出现反常,其原因是
(5)用高能射线照射液态H2A时,一个H2A分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式: 。写出该阳离子与硫的氢化物的水溶液反应的离子方程式:
A、B、C、D、E是周期表中前四周期的元素,其有关性质或结构信息如下表:
| 元素 | 有关性质或结构信息 |
| A | 负二价的A元素的氢化物在通常状况下是一种液体,其中A的质量分数为88.9% |
| B | B原子得到一个电子后3p轨道全充满 |
| C | C原子的p轨道半充满,它的气态氢化物能与其最高价氧化物的水化物反应生成一种常见的盐X |
| D | D元素的最高化合价与最低化合价的代数和为零,其最高价氧化物为分子晶体 |
| E | E元素的核电荷数等于A元素和B元素氢化物的核电荷数之和 |
A、B、C、D、E是周期表中前四周期的元素,其有关性质或结构信息如下表:
| 元素 | 有关性质或结构信息 |
| A | 负二价的A元素的氢化物在通常状况下是一种液体,其中A的质量分数为88.9% |
| B | B原子得到一个电子后3p轨道全充满 |
| C | C原子的p轨道半充满,它的气态氢化物能与其最高价氧化物的水化物反应生成一种常见的盐X |
| D | D元素的最高化合价与最低化合价的代数和为零,其最高价氧化物为分子晶体 |
| E | E元素的核电荷数等于A原子和B元素氢化物的核电荷数之和 |
A、B、C、D、E是周期表中前四周期的元素,其有关性质或结构信息如下表:
元素有关性质或结构信息
A负二价的A元素的氢化物在通常状况下是一种液体,其中A的质量分数为88.9%
BB原子得到一个电子后3p轨道全充满
CC原子的p轨道半充满,它的气态氢化物能与其最高价氧化物的水化物反应生成一种常见的盐X
DD元素的最高化合价与最低化合价的代数和为零,其最高价氧化物为分子晶体
EE元素的核电荷数等于A元素和B元素氢化物的核电荷数之和
(1)元素Y是C下一周期同主族元素,比较B、Y元素的第一电离能I1(B) I1(Y)。
(2)E元素原子的核外电子排布式为
(3)盐X的水溶液呈 (填“酸性”、“碱性”或“中性”),B元素最高价含氧酸一定比D元素最高价含氧酸的酸性 (填“强”或“弱”)。
(4)C单质分子中σ键和π键的个数比为 ,C的氢化物在同族元素的氢化物中沸点出现反常,其原因是
(5)用高能射线照射液态H2A时,一个H2A分子能释放出一个电子,同时产生一种具有较强氧化性的阳离子,试写出该阳离子的电子式: ,
写出该阳离子与硫的氢化物的水溶液反应的离子方程式:
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com