
题目列表(包括答案和解析)

图15-11
(1)Q内发生化学反应时,生成的气体是_____________。
(2)为了测定反应生成气体的总体积,滴加稀硫酸之前,K1、K2、K3中应当关闭的是__________,应当打开的是_____________。
(3)当上述反应停止,将K1、K2、K3均处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是__________________________________________________________。
(4)b中装的固体试剂是___________,为什么要缓缓打K1__________________________。
(5)实验结束时,量筒Ⅰ中有x mL水,量筒Ⅱ中收集到y mL气体(已折算成标准状况),则过氧化钠的纯度的数学表达式是__________________________(需化成最简表达式)。
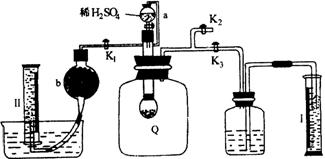
为了测定已部分变质的过氧化钠样品的纯度,设计右图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装好仪器,打开了漏斗的活塞,将稀硫酸滴入气球中。请填空:
|
(1)Q内发生化学反应时,生成的气体是 。
(2)为了测定反应生成气体的总体积,滴加稀硫酸之前,K1、K2、K3中应当关闭的是 ,应当打开的是 。
(3)当上述反应停止,将K1、K2、K3均处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是 。
(4)b中装的固体试剂是 ,为什么要缓缓打开K1 。
(5)实验结束时,量筒I中有x mL水,量筒II中收集到y mL气体(已折算成标准状态),则过氧化钠的纯度的数学表达式是 (需化成最简表达式。
(1)Q内发生化学反应时,生成的气体是__________________________________________。
(2)为了测定反应生成气体的总体积,滴加稀硫酸之前,K1、K2、K3中应当关闭的是_______________,应当打开的是_______________。
(3)当上述反应停止,将K1、K2、K3均处于关闭状态,然后先打开K2,再缓缓打开K1,这时可观察到的现象是__________________________________________。
(4)b中装的固体试剂是___________________________________________,为什么要缓缓打开K1?___________________________________________________________。
(5)实验结束时,量筒Ⅰ中有x mL水,量简Ⅱ中收集到y mL气体(已折算成标准状态),则过氧化钠的纯度的数学表达式是___________________________(化成最简表达式)。
| |||||||||||||||||||||||
试回答下列问题:
第一步:称取样品Ag,写出称量时用到的仪器的名称:________。
第二步:样品溶解,写出溶解时用到的仪器的名称:________。
第三步:在溶液中加入过量的盐酸,再加入过量的氯化钡溶液,①加入过量的盐酸的原因是________;②氯化钡溶液要过量的原因是________;③检验氯化钡是否过量的方法是________。
第四步:过滤和洗涤沉淀。①过滤时所用仪器与上述几步操作中所用的仪器重复的是________,作用是________。②所得沉淀若不经洗涤则导致实验测定值________。③洗涤沉淀的方法是________。
第五步:烘干沉淀并计算。
若烘干后的沉淀称量为Bg,计算样品中亚硫酸钠纯度为________。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com