
题目列表(包括答案和解析)
298K时,有两只容积相等的密闭容器A和B,A容器保持恒容,B容器保持恒压。起始时,向A容器充入3molH2和1molN2,向B容器充入3molH2和2molN2,发生如下反应:
N2(g)+3H2(g)![]() 2NH3(g)。已知298K时,
2NH3(g)。已知298K时,![]() H=-92.4kJ?mol-1,
H=-92.4kJ?mol-1,![]() S=-198.2J?mol-1?K-1
S=-198.2J?mol-1?K-1
请回答下列问题:
(1)根据反应的焓变和熵变计算分析298K下合成氨反应能自发进行(列出计算式即可)
(2)达平衡后,若向两容器中通入与起始时等量的原反应气体,达到新的平衡时,A容器中NH3的体积分数 (填“增大”、“减小”或“不变”,下同),B容器中的NH3的体积分数
(3)298K时,将NH3通入水中得到0.1mol?L-1的氨水,测定其pH约为11,向其中加入少量的NH4Cl晶体,晶体溶解后发现溶液的pH减小。对于上述现象有两种不同的解释:
甲观点:NH4Cl水解呈酸性,增大c(H+),因此溶液的pH减小。
乙观点:NH4Cl溶于水电离出大量的NH4+,抑制NH3?H2O的电离,使c(OH-)减小,因此溶液的pH减小。
请你设计一个简单实验进行验证上述观点哪个正确,试剂自选。
(提示:298K时,0.1mol?L-1的NH3?H2O和CH3COOH的电离常数均为1.75×10-5)
 等量的SO2和O2,使之发生反应:2SO2+O2
等量的SO2和O2,使之发生反应:2SO2+O2 2SO3,并达到平衡。试回答:
2SO3,并达到平衡。试回答: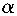 (A)_____
(A)_____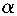 (B)。
(B)。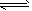 2SO3,并达到平衡。则(填>、=、<;“正”、“逆”、“不”;增大、减小、不变)。
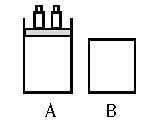
2SO3,并达到平衡。则(填>、=、<;“正”、“逆”、“不”;增大、减小、不变)。如图所示有两只密闭容器A和B,A容器有一个移动的活塞使容积内保持恒压,B容器能保持恒容,起始时向这两只容器中分别充入等量的体积比为2∶1的SO2和O2的混合气体,并使A和B容积相等.在保持400℃的条件下使之发生如下反应:2SO2+O2![]() 2SO3,填写下列空格.
2SO3,填写下列空格.
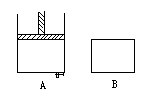
(1)达到平衡所需时间,A容器比B容器________,A容器SO2的转化率比B容器________.
(2)达到(1)所述平衡后,若向两容器中通入数量不多的等量氩气,A容积中v(正)________,v(逆)________,化学平衡____向移动;B容器中v(正)________,v(逆)________,化学平衡______向移动.
有两只密闭的容器A和B,A能保持恒压,B能保持恒容。起始时向容积相等的两容器中通入体积比为2:l的等量的S02和02,使之发生反应: 2S02 +02 ![]() 2S03,并达到平衡。则(填<、=、>;左、右;增大、减小、不变)
2S03,并达到平衡。则(填<、=、>;左、右;增大、减小、不变)
(1)达到平衡所需的时间:tA tB,S02的转化率:aA aB。
(2)起始时两容器中的反应速率:vA_______vB,反应过程中的反应速率:vA______vB
(3)达到平衡时,向两容器中分别通入等量的氩气。A容器中的化学平衡向 反应方向移动,B容器中的化学反应速率
(4)达到平衡后,向两容器中分别通入等量的原反应气体,再次达到平衡时,A容器中的S02的百分含量 ,B容器中S02的百分含量 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com