钛是继铁、铝后的第三金属,常温下钛的化学活性很小,仅能与氟气、氢氟酸等几种物质起作用.但在较高温度下,钛可与多种单质和化合物发生反应.工业上冶炼钛主要以钛铁矿、金红石(含TiO
2大于96%)等为原料生产.
(1)由金红石为原料采用亨特(Hunter)法生产钛的流程如下:

①沸腾氯化炉中反应:TiO
2(s)+2Cl
2 (g)=TiCl
4(l)+O
2(g),在常温下能否自发进行(已知该反应△H=184kJ/mol,△S=57.74J/K)
不能
不能
(选填:“能”或“不能”).
②已知:Ti(s)+2Cl
2(g)=TiCl
4(l)△H=-804.2kJ/mol;2Na(s)+Cl
2(g)=2NaCl(s)△H=-882.0kJ/mol;
Na(s)=Na(l)△H=2.6kJ/mol.
则TiCl
4(l)+4Na(l)=Ti(s)+4NaCl(s)△H=
-970.2
-970.2
kJ/mol
③海绵钛破碎后用0.5%~1.5%的盐酸洗涤,再用蒸馏水洗涤至中性,用盐酸洗涤的目的
除去其中过量的钠并溶解氯化钠及钛的低价氯化物
除去其中过量的钠并溶解氯化钠及钛的低价氯化物
.
(2)科学家从电解冶炼铝的工艺得到启发,找出了冶炼钛的新工艺.试回答下列有关问题.
①TiO
2直接电解法(剑桥法)生产钛是一种较先进的方法,电解质为熔融的氯化钙,原理如右图所示,

阴极获得钛可能发生的反应或电极反应为:
TiO2+4e-=Ti+O2-
TiO2+4e-=Ti+O2-
.
②SOM技术是一种绿色环保先进技术,阳极用金属陶瓷,并用固体氧离子隔膜将两极产物隔开,阳极通入某种还原性气体,可防止CO、CO
2污染物产生,通入的气体是
H2
H2
.
(3)海棉钛通常需要经过真空电弧炉里熔炼提纯,也可通过碘提纯法,原理为:

,下列说法正确的是
d
d
.
(a) 该反应正反应为的△H>0
(b) 在不同温度区域,TiI
4的量保持不变
(c) 在提纯过程中,I
2的量不断减少
(d) 在提纯过程中,I
2的作用是将粗钛从低温区转移到高温区.

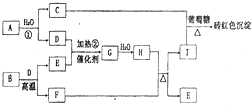 (2011?郑州二模)如图为物质A?I的转化关系(部分反应物、生成物没有列出).其中B为某金屑矿的主要成分,经过一系列反应可得到E和F.D、E常温下为气体,D、F为常见单质,
(2011?郑州二模)如图为物质A?I的转化关系(部分反应物、生成物没有列出).其中B为某金屑矿的主要成分,经过一系列反应可得到E和F.D、E常温下为气体,D、F为常见单质,
 阴极获得钛可能发生的反应或电极反应为:
阴极获得钛可能发生的反应或电极反应为: ,下列说法正确的是
,下列说法正确的是