
题目列表(包括答案和解析)
某工厂以乙炔为原料生产维尼纶的过程中,首先要合成一种中间体,其结构简式为: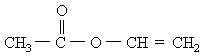
(1)该中间体的名称是________.
(2)该中间体可能进行下列哪些类型的反应
[ ]
(3)该中间体和稀NaOH溶液共热,可蒸馏出一种能发生银镜反应的有机物甲,写出该中间体和NaOH溶液反应的化学方程式:________
乙烯是石油化工的重要原料,它主要通过石油产品裂解获得。
(1)石油产品裂解所得裂解气的平均组成可表示为CnHm(m>2n),经测定某裂解气中各气体的体积分数分别为:甲烷―4%、乙烯―50%、丙烯―10%、其余为丁二烯和氢气(气体体积均在同温同压下测定)。若得到50 mol乙烯,x mol丁二烯和y mol氢气。则x+y= , n / m = (请用含x的式子表示)。
(2)某化工厂每天由石油产品裂解得到乙烯56 t。再以乙烯为主要原料生产醋酸乙烯酯,醋酸乙烯酯是合成维尼纶的重要单体。生产原理如下:
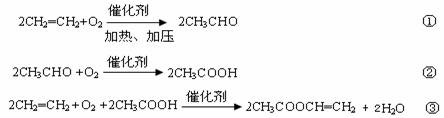
反应①中乙烯的利用率为80%,反应②中乙醛的利用率为83.33%,反应③中乙酸与乙烯的利用率均为85%。则该厂每天最多可制得醋酸乙烯酯多少吨?
(6分)在一定条件下,醇和醛能发生如下的反应:
R-OH+R’-![]() -H→R’-
-H→R’-![]() -OR(产物统称半缩醛)
-OR(产物统称半缩醛)
![]()
(1)已知葡萄糖溶液中,葡萄糖以链状分子和六元环半缩醛分子两种同分异构体形式平衡共存,相互转化。请写出葡萄糖环状分子的结构简式;
![]()
(2)聚乙烯醇(C2H4O)n与甲醛反应可生成含有六元环状结构的维尼纶(C5H8O2)n。
![]()
①写出化学方程式(有机物写结构简式);
![]()
②实际生产中用C4H6O2替代聚乙烯醇,写出化学式和名称
| 催化剂 |
| 催化剂 |
| 催化剂 |
| 1 |
| 5 |
| ||
| ||
| ||
| ||
| ||
| ||
| 1 |
| 2 |
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com