
题目列表(包括答案和解析)
(15分) 为省药品和时间,甲、乙、丙三位同学用铜片、锌片、铁片、稀H2SO4、NaCl溶液、ZnSO4溶液、CuSO4溶液;石墨电极、导线、烧杯、试管等中学化学常见的药品和仪器(用品),以巧妙的构思,“接力”的方式,利用不同原理分别设计了比较铜与锌金属活动性相对强弱的系列实验。试填写下列空白:
⑴甲同学分别将一小片铜片、锌片置于烧杯底部(铜与锌不接触),小心向烧杯中加入稀硫酸,观察到的现象是 。甲同学的设计思路是 。
⑵乙同学接着甲的实验,向烧杯中滴加 溶液,进而观察到的现象是 , 。乙同学作出锌、铜金属活动性相对强弱所依据的原理是 , 。
⑶丙同学认为在锌的表面镀铜可以有效防止锌的锈蚀,但如果镀铜层破损后,在潮湿的空气中反而加速锌的锈蚀,原因是在锌的表面构成了无数微小的原电池。试写出有关电极反应式:负极 ;正极 。
⑷请你利用题给药品与仪器,区别于甲、乙的设计原理,再设计一个简单的实验,证实锌和铜的金属活动性的相对强弱(简要说明操作和现象) 。
(08长沙雅礼中学二模)(15分)一种用于治疗高血脂的新药灭脂灵是按如下路线合成的:
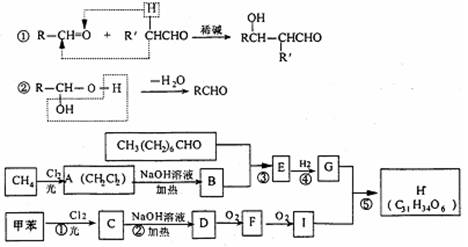 |
已知G的分子式为C10H22O3,试回答:
(1)写出B、E结构简式:_________ 、________ ;
(2)上述反应中属于取代反应的是_______________________(填序号);
(3)写出下列反应的化学方程式:
I、反应② ;
Ⅱ、F与银氨溶液反应: 。
(4)I的同分异构体 (填结构简式)符合下列三个条件:
①遇FeCl3溶液呈紫色 ②与新制的Cu(OH)2共热产生红色沉淀
③苯环上的一取代物只有二种。
(15分)C、Si、S和N元素在化学中占有极其重要的地位。
 (1)写出Si的基态原子价电子排布式
。
(1)写出Si的基态原子价电子排布式
。
从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为 。
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为 ,微粒间存在的作用力是 。
(3)氧化物MO的电子总数与SiC的相等,MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是 。
 (4)SO2、NO2、H2S同属于
结构(填“三角锥形”、“直线型”或“V字型”)。从微观结构角度分析,其中一种分子又与另二种分子有不同之处,该分子的化学式是
。
(4)SO2、NO2、H2S同属于
结构(填“三角锥形”、“直线型”或“V字型”)。从微观结构角度分析,其中一种分子又与另二种分子有不同之处,该分子的化学式是
。
(15分)C、Si、S和N元素在化学中占有极其重要的地位。 (1)写出Si的基态原子价电子排布式 。
(1)写出Si的基态原子价电子排布式 。
从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为 。 (2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为 ,微粒间存在的作用力是 。
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为 ,微粒间存在的作用力是 。
(3)氧化物MO的电子总数与SiC的相等,MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是 。 (4)SO2、NO2、H2S同属于 结构(填“三角锥形”、“直线型”或“V字型”)。从微观结构角度分析,其中一种分子又与另二种分子有不同之处,该分子的化学式是 。
(4)SO2、NO2、H2S同属于 结构(填“三角锥形”、“直线型”或“V字型”)。从微观结构角度分析,其中一种分子又与另二种分子有不同之处,该分子的化学式是 。
(15分)C、Si、S和N元素在化学中占有极其重要的地位。
(1)写出Si的基态原子价电子排布式 。
从电负性角度分析,C、Si和O元素的非金属活泼性由强至弱的顺序为 。
(2)SiC的晶体结构与晶体硅的相似,其中C原子的杂化方式为 ,微粒间存在的作用力是 。
(3)氧化物MO的电子总数与SiC的相等,MO是优良的耐高温材料,其晶体结构与NaCl晶体相似。MO的熔点比CaO的高,其原因是 。
(4)SO2、NO2、H2S同属于 结构(填“三角锥形”、“直线型”或“V字型”)。从微观结构角度分析,其中一种分子又与另二种分子有不同之处,该分子的化学式是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com