
题目列表(包括答案和解析)
将一定量的铁粉和硫粉的混合物隔绝空气共热,充分反应后冷却,再加入足量稀 ,得标准状况下气体11.2L,则原混合物可能的组成是________.(n代表物质的量)
,得标准状况下气体11.2L,则原混合物可能的组成是________.(n代表物质的量)
[ ]
|
A.n(Fe)<n(S)总质量等于44g |
B.n(Fe)>n(S)总质量等于44g |
|
C.n(Fe)=n(S)总质量大于44g |
D.n(Fe)>n(S)总质量小于44g |
将一定量的混合均匀的铁粉和硫粉在隔绝空气的条件下共热,充分反应后冷却至室温,得到固体A.将质量为m的固体A加入到300 mL 2 mol·L-1盐酸中使之完全溶解,测得室温下加入的固体A的质量与收集到的气体体积(已换算成标准状况)的关系如图,(假设氢硫酸溶液饱和之前无硫化氢逸出).已知加入固体A的质量m≤3.2 g时,收集到的气体为氢气,当m>3.2 g时收集到的气体为氢气和硫化氢的混合气.
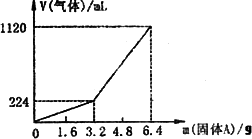
试分析与计算:
(1)3.2 g固体A中所含的物质有(写化学式)________.
(2)3.2 g固体A中各物质的物质的量分别为________.溶于上述盐酸充分反应后,所得的溶液中氢硫酸的物质的量浓度为(忽略体积变化)________.
(3)当固体A全部溶于上述盐酸,且A的质量m>3.2 g时,收集到的气体体积(标准状况下)V=________mL.(用含m的代数式)
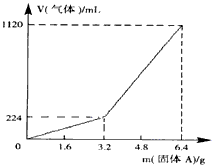

已知加入固体A的质量m≤3.2 g时,收集到的气体为氢气;当m>3.2 g时,收集到的气体为H2和H2S的混合气体。
试分析计算:
(1)3.2 g固体A中所含的物质有_____________。
(2)3.2 g固体A中各物质的物质的量分别为_______________,溶于上述盐酸充分反应后,所得溶液中氢硫酸的物质的量浓度为(忽略溶液体积的变化)______________。
(3)当固体A全部溶于上述盐酸,且A的质量m>3.2 g时,收集到气体体积(标准体积)V=____________mL(用含m的代数式表示)。
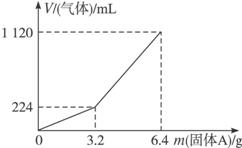
(1)3.2 g固体A中所含的物质有__________;各物质的物质的量分别为__________,溶于上述盐酸充分反应后,所得溶液中溶质的物质的量浓度为(忽略溶液体积变化)__________。
(2)当固体A全部溶于上述盐酸,且A的质量m>3.2 g时,收集到的气体体积(标准状况下)V=__________mL(用含m的代数式表示)。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com