
题目列表(包括答案和解析)
(共9分) (1) 谷氨酸的系统名为:2-氨基戊二酸(pKa1=2.19,pKa2=4.25,pKa3=9.67)。请回答下列问题:
① 写出其结构式 ;
② 写出谷氨酸在pH=10.00的水溶液中,占优势的离子结构 ;
③ 若谷氨酸溶于pH=7的纯水中,所得溶液的pH是x,则x 7(填“>”或“<”);此氨基酸等电点是大于x还是小于x?为什么?
。
(2) 110.1℃,6.050×104Pa,测定醋酸蒸气的密度所得到的平均相对摩尔质量是醋酸单分子摩尔质量的1.520倍。假定气体中只含有单分子和双分子。则110.1℃下反应2CH3COOH(g)![]() (CH3COOH)2(g)的
(CH3COOH)2(g)的![]() 为 ;
为 ;![]() 的计算公式及结果为:(
的计算公式及结果为:(![]() =1.013×105Pa) 。
=1.013×105Pa) 。
(本题共9分)化学能在一定的条件下可以转化为电能。
(一)现有如下两个反应:
① 2FeCl3 + Cu = 2FeCl2 + CuCl2
② Na2CO3 + 2HCl = 2NaCl + H2O + CO2↑
(1)根据两个反应的本质判断,您认为可以设计成原电池的是 (填反应序号),理由是 。
(二)请根据Zn + CuSO4 = ZnSO4 + Cu反应,选择适宜的材料和试剂设计一个原电池。
(2)画出原电池装置图,并在图中标注出电极和电解质溶液的名称。
(3)写出该原电池电极反应式:正极: ;负极: 。
(共9分,每空1分)物质在水中可能存在电离平衡、盐的水解平衡和沉淀的溶解平衡,它们都可看作化学平衡。请根据所学知识的回答:
(1)A为0.1 mol·L-1的(NH4)2SO4溶液,在该溶液中各种离子的浓度由大到小顺序为
。
(2)B为0.1 mol·L-1NaHCO3溶液,在NaHCO3溶液中存在的各种平衡体系为(用离子方
程式表示): ; ;
实验测得NaHCO3溶液的pH > 7,请分析NaHCO3溶液显碱性的原因:
。
(3)C为FeCl3溶液,实验室中配制FeCl3溶液时通常需要向其中加入 ,目的是 ;
若把B和C溶液混合,将产生红褐色沉淀和无色气体,该反应的离子方程式为
。
(4)D为含有足量AgCl固体的饱和溶液,氯化银在水中存在沉淀溶解平衡:
AgCl(S)  Ag+(aq)+ Cl-(aq) 在25℃时,氯化银的Ksp = 1.8×10-10
Ag+(aq)+ Cl-(aq) 在25℃时,氯化银的Ksp = 1.8×10-10
25℃时,现将足量氯化银分别放入:①100mL蒸馏水中;②100mL 0.2 mol·L-1AgNO3溶液中;③100mL 0.1 mol·L-1氯化铝溶液中;④100mL 0.1 mol·L-1盐酸溶液中。充分搅抖后,相同温度下银离子浓度由大到小的顺序是 (填写序号);②中氯离子的浓度为 mol·L-1
(每空3分,共9分)在一定条件下,反应 达到平衡。
达到平衡。
(1)若A、B、C都是气体,在增压后平衡向逆反应方向移动,则,y,之间的关系是 。
(2)若C是气体,且+y=,在增大压强时,如果平衡发生移动,则A的转化率将 (填“增大”、 “减小”或“不变”)
(3)若A为固体,B、C为气体,且y>,则增大压强时混和气体的平均相对分子质量将 (填“增大”“减小”或“不变”)
(每小题3分,共9分)恒温恒压下,在一个容积可变的密闭容器中发生如下反应:
(1)若开始时通入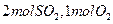 ,达平衡时生成
,达平衡时生成 的转化率为 。
的转化率为 。
(2)若开始时通入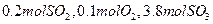 ,达平衡时SO2的物质的量为 mol。
,达平衡时SO2的物质的量为 mol。
(3)若在(2)的平衡混合物中再通入bmol SO3,则达到平衡时SO3的体积分数是 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com