
题目列表(包括答案和解析)
| A、c(H+) | B、c(OH-) | C、c(H2PO4-) | D、Kw |
(15分)、对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。若25℃时有HA H++A―,则K=
H++A―,则K= 。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。
。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。
回答下列问题:
(1)当升高温度时,K值____(填“变大”“变小”或“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系? ____ ________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、
H2PO4-、HPO42-都看做是酸,其中酸性最强的是_ ,最弱的是_ __。
(4)同一多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是_____________,产生此规律的原因是_____________ ___。
(5) Na2CO3溶液呈_ _(填“酸性”“碱性”或“中性”),其原因(用离子方程式表示)是_ 。
(6)已知NaH2PO4溶液呈酸性,则该溶液中c(H3PO4)____c(HPO42-)(填“大于”或“小于” )。
A.[H+] B.[OH-] C.[![]() ] D.KW
] D.KW
已知NaH2PO4溶液呈酸性,在水溶液中存在如下水解平衡:H2PO-4+H2O![]() H3PO4+OH-,现将0.1 mol·L-1NaH2PO4溶液稀释后,增大的是( )
H3PO4+OH-,现将0.1 mol·L-1NaH2PO4溶液稀释后,增大的是( )
A.[H+] B.[OH-] C.[![]() ] D.KW
] D.KW
(15分)、对于弱酸,在一定温度下达到电离平衡时,各微粒的浓度存在一种定量的关系。若25℃时有HA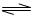 H++A―,则K=
H++A―,则K= 。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。
。式中:K为电离平衡常数,只与温度有关,c为各微粒的平衡浓度。下表是几种常见弱酸的电离平衡常数(25℃)。

回答下列问题:
(1)当升高温度时,K值____(填“变大”“变小”或“不变”)。
(2)在温度相同时,各弱酸的K值不同,那么K值的大小与酸性的相对强弱有何关系? ____ ________。
(3)若把CH3COOH、H2CO3、HCO3-、H2S、HS-、H3PO4、
H2PO4-、HPO42-都看做是酸,其中酸性最强的是_ ,最弱的是_ __。
(4)同一多元弱酸的K1、K2、K3之间存在着数量上的规律,此规律是_____________,产生此规律的原因是_____________ ___。
(5) Na2CO3溶液呈_ _(填“酸性”“碱性”或“中性”),其原因(用离子方程式表示)是_ 。
(6)已知NaH2PO4溶液呈酸性,则该溶液中c(H3PO4)____c(HPO42-)(填“大于”或“小于” )。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com