
题目列表(包括答案和解析)
为验证卤素单质氧化性的相对强弱,某小组用右图所示装置进行试验(夹持仪器已略去,气密性已检验)。试验过程:
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.当B中溶液由黄色变为棕色时,关闭活塞a。
IV.……
试回答下列问题:
(1)A中产生 色气体,其结构式是 。
(2)能使湿润的淀粉—KI试纸变蓝的气体是 。
(a) Cl2(b) N2O4 (c) I2蒸气 (d) SO2 (e) O3 (f) CO2
(3)滴加浓盐酸前,分液漏斗首先要 。
(4)过程III实验目的是 。
(5)A中产生氯气的离子方程式为 。
(6)B中浸有NaOH溶液的棉花作用是 ,写出反应的离子方程式 。
为验证卤素单质氧化性的相对强弱,某小组用右图所示装置进行试验(夹持仪器已略去,气密性已检验)。试验过程: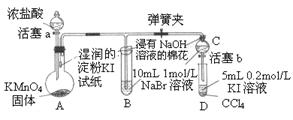
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.当B中溶液由黄色变为棕色时,关闭活塞a。
IV.……
试回答下列问题:
(1)A中产生 色气体,其结构式是 。
(2)能使湿润的淀粉—KI试纸变蓝的气体是 。
(a) Cl2 (b) N2O4 (c) I2蒸气 (d) SO2 (e) O3 (f) CO2
(3)滴加浓盐酸前,分液漏斗首先要 。
(4)过程III实验目的是 。
(5)A中产生氯气的离子方程式为 。
(6)B中浸有NaOH溶液的棉花作用是 ,写出反应的离子方程式 。
为验证卤素单质氧化性的相对强弱,某小组用右图所示装置进行试验(夹持仪器已略去,气密性已检验)。试验过程:
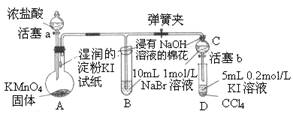
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.当B中溶液由黄色变为棕色时,关闭活塞a。
IV.……
试回答下列问题:
(1)A中产生 色气体,其结构式是 。
(2)能使湿润的淀粉—KI试纸变蓝的气体是 。
(a) Cl2 (b) N2O4 (c) I2蒸气 (d) SO2 (e) O3 (f) CO2
(3)滴加浓盐酸前,分液漏斗首先要 。
(4)过程III实验目的是 。
(5)A中产生氯气的离子方程式为 。
(6)B中浸有NaOH溶液的棉花作用是 ,写出反应的离子方程式 。
为验证卤素单质氧化性的相对强弱,某小组用右图所示装置进行试验(夹持仪器已略去,气密性已检验)。试验过程:
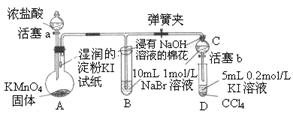
I.打开弹簧夹,打开活塞a,滴加浓盐酸。
II.当B和C中的溶液都变为黄色时,夹紧弹簧夹。
III.当B中溶液由黄色变为棕色时,关闭活塞a。
IV.……
试回答下列问题:
(1)A中产生 色气体,其结构式是 。
(2)能使湿润的淀粉—KI试纸变蓝的气体是 。
(a) Cl2 (b) N2O4 (c) I2蒸气 (d) SO2 (e) O3 (f) CO2
(3)滴加浓盐酸前,分液漏斗首先要 。
(4)过程III实验目的是 。
(5)A中产生氯气的离子方程式为 。
(6)B中浸有NaOH溶液的棉花作用是 ,写出反应的离子方程式 。
 (2011?德州二模)工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用该原理处理污水,设计装置示意图.如图所示.
(2011?德州二模)工业上采用的一种污水处理方法如下:保持污水的pH在5.0~6.0之间,通过电解生成Fe(OH)3沉淀.Fe(OH)3有吸附性,可吸附污物而沉积下来,具有净化水的作用.阴极产生的气泡把污水中悬浮物带到水面形成浮渣层,刮去(或撇掉)浮渣层,即起到了浮选净化的作用.某科研小组用该原理处理污水,设计装置示意图.如图所示.
| ||
| ||
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com