
题目列表(包括答案和解析)

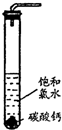 实验一、定性探究:
实验一、定性探究: HClO+HCl,加入过量的CaCO3与溶液中的HCl发生反应,使盐酸的浓度减小,平衡向正反应方向移动,最终生成HClO
HClO+HCl,加入过量的CaCO3与溶液中的HCl发生反应,使盐酸的浓度减小,平衡向正反应方向移动,最终生成HClO HClO+HCl,加入过量的CaCO3与溶液中的HCl发生反应,使盐酸的浓度减小,平衡向正反应方向移动,最终生成HClO
HClO+HCl,加入过量的CaCO3与溶液中的HCl发生反应,使盐酸的浓度减小,平衡向正反应方向移动,最终生成HClO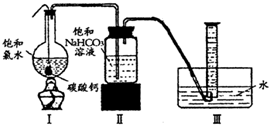
| BL |
| 22.4L/mol |
| Ag |
| 100g/mol |
(1)浓盐酸在反应中显示出来的性质是_____________。
A.只有还原性 B.还原性和酸性
C.只有氧化性 D.氧化性和酸性
(2)产生0.1 mol Cl2,则转移的电子的物质的量为_____________mol。
(3)ClO2具有很强的氧化性,因此常被用作消毒剂,若ClO2、Cl2消毒后均变为Cl-,则ClO2的消毒效率(以单位质量得到的电子数表示)是Cl2的_____________倍。
KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯.其变化可表述为:
aKClO3+bHCl(浓)——cKCl+dClO2+eCl2↑+fH2O
(1)、浓盐酸在反应中显示出来的性质为________、________;还原产物为(填名称)________.
(2)、根据Cl元素守恒得a、b、c、的关系式为________.
(3)、产生2 mol ClO2,则转移的电子的物质的量为________ mol.
(4)、写出该反应的离子方程式________.
KClO3和浓盐酸在一定温度下反应会生成绿黄色的易爆物二氧化氯.其变化可表述为:
aKClO3+bHCl(浓)——cKCl+dClO2+eCl2↑+fH2O
(1)浓盐酸在反应中显示出来的性质________、________;还原产物为________.
(2)根据Cl元素守恒得a、b、c、d、e的关系式为________________________.
(3)产生2 mol ClO2,则转移的电子的物质的量为____________mol.
(4)写出该反应的离子方程式________________________________.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com