
题目列表(包括答案和解析)
Ⅰ.某矿样含有大量的CuS、少量铁的氧化物及少量其它不溶于酸的杂质。某化学课外小组设计以下流程,以该矿样为原料生产CuCl2·2H2O晶体。

(1)在焙烧过程产生的尾气中,有一种是主要的大气污染物。若在实验室中以碱液吸收处理之,下列装置可行的是_________(填字母)。

(2)步骤②酸浸过程中,需要用到3mol·L-1,的盐酸100mL,配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有_________________________;
(3)步骤④中,加入的X物质可以是________,作用是_____________。
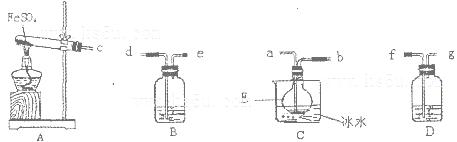
Ⅱ.已知FeSO4在高温下分解生成Fe2O3、SO3和SO2用下图所示装置设计实验,检验FeSO4在高温下分解生成的气态物质,并测定已分解的FeSO4质量.

已知:B装置、烧瓶E中所加试剂依次为氢氧化钠溶液、水(滴有数滴BaCl2溶液),请回答下列问题:
(1)D装置中所加试剂名称_____________________________________________。
(2)按气流方向连接各仪器,用字母表示接口的连接顺序:c→_______________→e。
(3)检验后,用烧瓶E中混合物测定已分解的FeSO4质量,此实验操作的第一步:_______________________________________________________;第二步:过滤混合物,在过滤器上将沉淀洗净后,灼烧并冷却至室温,称量其质量为ag,再次灼烧冷却至室温称量其质量为bg,且b<a,继续灼烧、冷却并称重,直到连续两次称量的质量差不超过0.1g为止。
(4)若最终得到沉淀cg,则已经分解的FeSO4质量________________(填计算式)。
Ⅰ.某矿样含有大量的CuS、少量铁的氧化物及少量其它不溶于酸的杂质。某化学课外小组设计以下流程,以该矿样为原料生产CuCl2·2H2O晶体。
(1)在焙烧过程产生的尾气中,有一种是主要的大气污染物。若在实验室中以碱液吸收处理之,下列装置可行的是_________(填字母)。
(2)步骤②酸浸过程中,需要用到3mol·L-1,的盐酸100mL,配制该盐酸溶液时,除了用到烧杯、玻璃棒、胶头滴管外,还需要的仪器有_________________________;
(3)步骤④中,加入的X物质可以是________,作用是_____________。
Ⅱ.已知FeSO4在高温下分解生成Fe2O3、SO3和SO2用下图所示装置设计实验,检验FeSO4在高温下分解生成的气态物质,并测定已分解的FeSO4质量.
已知:B装置、烧瓶E中所加试剂依次为氢氧化钠溶液、水(滴有数滴BaCl2溶液),请回答下列问题:
(1)D装置中所加试剂名称_____________________________________________。
(2)按气流方向连接各仪器,用字母表示接口的连接顺序:c→_______________→e。
(3)检验后,用烧瓶E中混合物测定已分解的FeSO4质量,此实验操作的第一步:_______________________________________________________;第二步:过滤混合物,在过滤器上将沉淀洗净后,灼烧并冷却至室温,称量其质量为ag,再次灼烧冷却至室温称量其质量为bg,且b<a,继续灼烧、冷却并称重,直到连续两次称量的质量差不超过0.1g为止。
(4)若最终得到沉淀cg,则已经分解的FeSO4质量________________(填计算式)。


湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com