
题目列表(包括答案和解析)
某小组同学欲制备SO2并探究其性质:
(一)实验室中需要SO2气体22.4 L(标准状况)。依据化学方程式Zn + 2 H2SO4(浓)![]() ZnSO4 + SO2↑ + 2 H2O计算后,取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g/mL)110 mL充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有杂质。
ZnSO4 + SO2↑ + 2 H2O计算后,取65.0 g锌粒与98%的浓H2SO4(ρ=1.84 g/mL)110 mL充分反应,锌全部溶解。对于制得的气体,有同学认为可能混有杂质。
(1)所制得的气体中混有的杂质气体可能是 (填分子式)。产生这种杂质的主要原因是 (用化学方程式表达)。
(2)为证实相关分析,组装了如下装置,对所制取的气体进行探究。
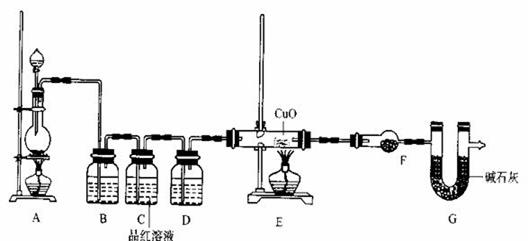
①装置B中加入的试剂是 ,作用是 。
②装置D中加入的试剂是 ,装置F中加入的试剂 是 。
③可证实一定量的锌粒和一定量的浓硫酸反应后生成的气体中混有该杂质气体的实验现象是 。
(二)利用下图所示的装置探究S![]() O2的性质:
O2的性质:
已知:熔点![]() :SO2 - 76.1℃,SO3 16.8℃;沸点:SO2 - 10℃,SO3 45℃
:SO2 - 76.1℃,SO3 16.8℃;沸点:SO2 - 10℃,SO3 45℃
| |
|
|
(1)装置I模拟工业生产SO3的反应,其化学方程式是 。
(2)甲同学按I、II、III、IV的顺序连接装置,装置II的作用是
;装置III中溶液![]() 逐渐褪色,有Mn2+生成,同时溶液酸性
逐渐褪色,有Mn2+生成,同时溶液酸性![]() 增强,则该反应的离子方程式是 。
增强,则该反应的离子方程式是 。
(3)乙同学按I、II、IV的顺序连接装置,若装置IV中有40 mL 2.5 mol??L-1 NaOH溶液,反应后溶液增重 4.8 g,则反应后溶液中含有的溶质有
(填化学式),对应溶质物质的量之比为 。
某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如下图所示的实验装置。
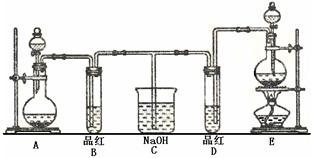
(1)实验室常选用制CO2的发生装置制SO2;实验室在用MnO2跟浓盐酸反应制备Cl2时,应选用上图A、E两发生装置中 ▲ 装置(填装置序号)制Cl2。在制Cl2的反应中浓盐酸所表现出的性质是 ▲ 。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个
试管加热,两个试管中的现象分别为B: ▲ ,D: ▲ 。
(3)装置C的作用是 ▲ 。
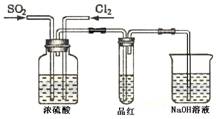
(4)甲乙两名同学分别利用下图所示装置探究两种气体按不同比例混合后的漂白性。试分析:
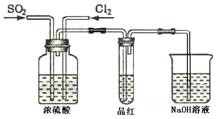
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是: ▲ 。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是: ▲ ,并写出其相应的离子方程式: ▲ 。
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅,其原因是: ▲ 。
(14分)某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如下图所示的实验装置。
(1)实验室常选用制CO2的发生装置制SO2;实验室在用MnO2跟浓盐酸反应制备Cl2时,应选用上图A、E两发生装置中 ▲ 装置(填装置序号)制Cl2。在制Cl2的反应中浓盐酸所表现出的性质是 ▲ 。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个
试管加热,两个试管中的现象分别为B: ▲ ,D: ▲ 。
(3)装置C的作用是 ▲ 。
(4)甲乙两名同学分别利用下图所示装置探究两种气体按不同比例混合后的漂白性。试分析:
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是: ▲ 。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是: ▲ ,并写出其相应的离子方程式: ▲ 。
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅,其原因是: ▲ 。
(14分)某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如下图所示的实验装置。
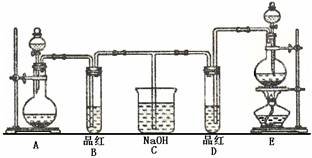
(1)实验室常选用制CO2的发生装置制SO2;实验室在用MnO2跟浓盐酸反应制备Cl2时,应选用上图A、E两发生装置中 ▲ 装置(填装置序号)制Cl2。在制Cl2的反应中浓盐酸所表现出的性质是 ▲ 。
(2)反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个
试管加热,两个试管中的现象分别为B: ▲ ,D: ▲ 。
(3)装置C的作用是 ▲ 。
(4)甲乙两名同学分别利用下图所示装置探究两种气体按不同比例混合后的漂白性。试分析:
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是: ▲ 。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是: ▲ ,并写出其相应的离子方程式: ▲ 。
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅,其原因是: ▲ 。
(12分)
Ⅰ.(3分)化学反应经常伴随着颜色变化,下列有关反应显示的颜色正确的有
①氢氧化亚铁在空气中最终变为灰绿色; ②淀粉溶液遇碘化钾变为蓝色;
③向硫酸铁溶液中加入KSCN变为红色 ④品红溶液通入过量氯气后褪色
⑤无水硫酸铜吸收水蒸气变成浅绿色; ⑥新制氯水久置后变为无色;
Ⅱ.(9分)某化学实验小组同学为了证明、比较SO2和氯水的漂白性,设计了如下图所示的实验装置。
(1) 实验室常选用制CO2的发生装置制SO2;实验室在用MnO2跟浓盐酸反应制备Cl2时,应选用上图A、E两发生装置中 装置(填装置序号)制Cl2。在制Cl2的反应中MnO2表现出的性质是 。
(2) 反应开始后,发现B、D两个试管中的品红溶液都褪去,停止通气后,给B、D两个
试管加热,两个试管中的现象分别为B: ,D: 。
(3) 装置C的作用是 。
(4) 甲乙两同学分别利用下图所示装置探究两种气体按不同比例混合后的漂白性。试分析:
①在气体进入品红溶液之前,先将SO2和Cl2通过盛有浓硫酸装置的目的是: 。
②甲同学在实验过程中发现:通气一段时间后,品红溶液几乎不褪色,其原因是: ,并写出其相应的离子方程式: 。
③乙同学在实验过程中发现:通气一段时间后,品红溶液颜色随时间推移变得越来越浅,其原因是: 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com