
ЬтФПСаБэ(АќРЈД№АИКЭНтЮі)
ЃЈ12ЗжЃЌУППе2ЗжЃЉ
ЕБНёЪРНчЃЌФмдДЕФЗЂеЙШевцГЩЮЊШЋЪРНчЁЂШЋШЫРрЙВЭЌЙиаФЕФЮЪЬтЁЃ
(1)AКЭBЕФЕЅжЪЕЅЮЛжЪСПЕФШМЩеШШДѓЃЌПЩгУзїШМСЯЁЃвбжЊAКЭBЮЊЖЬжмЦкдЊЫиЃЌЦфдзгЕФЕквЛжСЕкЫФЕчРыФмШчЯТБэЫљЪОЃК
|
ЕчРыФм(kJ/mol) |
I1 |
I2 |
I3 |
I4 |
|
A |
899 |
1 757 |
14 840 |
21 000 |
|
B |
738 |
1 451 |
7 733 |
10 540 |
ЂйЧыИљОнЩЯЪіаХЯЂЃЌаДГіAЛљЬЌдзгЕФКЫЭтЕчзгХХВМЪНЃК__________________ЁЃ
ЂкФГЭЌбЇИљОнЩЯЪіаХЯЂЃЌЭЦЖЯBЕФКЫЭтЕчзгХХВМШчЭМ1ЫљЪОЃЌИУЭЌбЇЫљЛЕФЕчзгХХВМЭМЮЅБГСЫ______________________ЁЃ
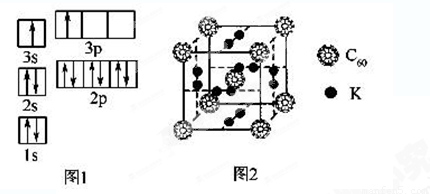
(2)ЧтЦјзїЮЊвЛжжЧхНрФмдДЃЌБиаыНтОіЫќЕФДЂДцЮЪЬтЃЌC60ПЩгУзїДЂЧтВФСЯЁЃ
ЂйвбжЊН№ИеЪЏжаCЁЊCМќЕФМќГЄЮЊ154.45 pmЃЌC60жаCЁЊCМќЕФМќГЄЮЊ145 pmКЭ140 pmЃЌгаЭЌбЇОнДЫШЯЮЊC60ЕФШлЕуИпгкН№ИеЪЏЃЌФуШЯЮЊЪЧЗёе§ШЗВЂВћЪіРэгЩ____________________________ ________________ЁЃ
ЂкПЦбЇМвАбC60КЭKВєдгдквЛЦ№жЦдьСЫвЛжжИЛРеЯЉЛЏКЯЮяЃЌЦфОЇАћШчЭМ2ЫљЪОЃЌИУЮяжЪдкЕЭЮТЪБЪЧвЛжжГЌЕМЬхЁЃИУЮяжЪжаKдзгКЭC60ЗжзгЕФИіЪ§БШЮЊ______________________ЁЃ
ЂлМЬC60КѓЃЌПЦбЇМвгжКЯГЩSi60ЁЂN60ЃЌCЁЂSiЁЂNдзгЕчИКадгЩДѓЕНаЁЕФЫГађЪЧ__________ ЁЃSi60ЗжзгжаУПИіЙшдзгжЛИњЯрСкЕФ3ИіЙшдзгаЮГЩЙВМлМќЃЌЧвУПИіЙшдзгзюЭтВуЖМТњзу8ЕчзгЮШЖЈНсЙЙЃЌдђSi60ЗжзгжаІаМќЕФЪ§ФПЮЊ______ЁЃ
(16Зж)IЁЂЮЊМѕЩйЮТЪваЇгІЃЌПЦбЇМвЩшМЦЗДгІЃКCO2+4H2==CH4+2H2OвдМѕаЁПеЦјжаCO2ЁЃ
ЃЈ1ЃЉШєга1mol CH4ЩњГЩЃЌдђга mol ІвМќКЭ mol ІаМќЖЯСбЁЃ
ЃЈ2ЃЉCH4ЪЇШЅHЁЊЃЈЧтИКРызгЃЉаЮГЩCH+3ЃЈМзЛље§РызгЃЉЁЃвбжЊCH+3ЕФПеМфНсЙЙЪЧЦНУце§Ш§НЧаЮЃЌдђCH+3жаЬМдзгЕФдгЛЏЗНЪНЮЊ ЁЃ
ЂђЁЂН№ЪєдзггыCOаЮГЩЕФХфКЯЮяГЦЮЊН№ЪєєЪЛљХфКЯЮяЃЈШчєЪЛљЬњЃЉЁЃаЮГЩХфКЯЮяЪБЃЌУПИіCOЬсЙЉвЛЖдЕчзггыН№ЪєдзгаЮГЩХфЮЛМќЃЌЧвН№ЪєдзгЕФМлЕчзгКЭCOЬсЙЉЕФЕчзгзмКЭЕШгк18ЁЃ
ЃЈ3ЃЉН№ЪєєЪЛљХфКЯЮяжаЃЌЮЂСЃМфзїгУСІга ЃЈЬюзжФИДњКХЃЉЁЃ
aЁЂРызгМќ bЁЂЙВМлМќ cЁЂХфЮЛМќ dЁЂН№ЪєМќ
ЃЈ4ЃЉєЪЛљЬњЪЧвЛжжЛЦЩЋгЭзДвКЬхЃЌШлЕуЃ21ЁцЁЂЗаЕу102.8ЁцЁЃгЩДЫЭЦВтЃЌЙЬЬхєЪЛљЬњИќНгНќгк ЃЈЬюОЇЬхРраЭЃЉЁЃШєгУFe(CO)xБэЪОєЪЛљЬњЕФЛЏбЇЪНЃЌдђx= ЁЃ
IIIЃЎбаОПБэУїЃЌЖдгкжааФРызгЮЊHg2+ЕШбєРызгЕФХфКЯЮяЃЌШєХфЮЛЬхИјГіЕчзгФмСІдНЧПЃЌдђХфЮЛЬхгыжааФРызгаЮГЩЕФХфЮЛМќОЭдНЧПЃЌХфКЯЮявВОЭдНЮШЖЈЁЃ
ЃЈ5ЃЉдЄВтHgCl42ЃгыHgI42ЃЕФЮШЖЈадЧПШѕЃЌВЂДгдЊЫиЕчИКадЕФНЧЖШМгвдНтЪЭЁЃ
Д№ЃКHgCl42ЃБШHgI42ЃИќ ЃЈЬюЁАЮШЖЈЁБЛђЁАВЛЮШЖЈЁБЃЉЃЌвђЮЊ ЁЃ
(16Зж)IЁЂЮЊМѕЩйЮТЪваЇгІЃЌПЦбЇМвЩшМЦЗДгІЃКCO2+4H2==CH4+2H2OвдМѕаЁПеЦјжаCO2ЁЃ
ЃЈ1ЃЉШєга1mol CH4ЩњГЩЃЌдђга mol ІвМќКЭ mol ІаМќЖЯСбЁЃ
ЃЈ2ЃЉCH4ЪЇШЅHЁЊЃЈЧтИКРызгЃЉаЮГЩCH+3ЃЈМзЛље§РызгЃЉЁЃвбжЊCH+3ЕФПеМфНсЙЙЪЧЦНУце§Ш§НЧаЮЃЌдђCH+3жаЬМдзгЕФдгЛЏЗНЪНЮЊ ЁЃ
ЂђЁЂН№ЪєдзггыCOаЮГЩЕФХфКЯЮяГЦЮЊН№ЪєєЪЛљХфКЯЮяЃЈШчєЪЛљЬњЃЉЁЃаЮГЩХфКЯЮяЪБЃЌУПИіCOЬсЙЉвЛЖдЕчзггыН№ЪєдзгаЮГЩХфЮЛМќЃЌЧвН№ЪєдзгЕФМлЕчзгКЭCOЬсЙЉЕФЕчзгзмКЭЕШгк18ЁЃ
ЃЈ3ЃЉН№ЪєєЪЛљХфКЯЮяжаЃЌЮЂСЃМфзїгУСІга ЃЈЬюзжФИДњКХЃЉЁЃ
aЁЂРызгМќ bЁЂЙВМлМќ cЁЂХфЮЛМќ dЁЂН№ЪєМќ
ЃЈ4ЃЉєЪЛљЬњЪЧвЛжжЛЦЩЋгЭзДвКЬхЃЌШлЕуЃ21ЁцЁЂЗаЕу102.8ЁцЁЃгЩДЫЭЦВтЃЌЙЬЬхєЪЛљЬњИќНгНќгк ЃЈЬюОЇЬхРраЭЃЉЁЃШєгУFe(CO)xБэЪОєЪЛљЬњЕФЛЏбЇЪНЃЌдђx= ЁЃ
IIIЃЎбаОПБэУїЃЌЖдгкжааФРызгЮЊHg2+ЕШбєРызгЕФХфКЯЮяЃЌШєХфЮЛЬхИјГіЕчзгФмСІдНЧПЃЌдђХфЮЛЬхгыжааФРызгаЮГЩЕФХфЮЛМќОЭдНЧПЃЌХфКЯЮявВОЭдНЮШЖЈЁЃ
ЃЈ5ЃЉдЄВтHgCl42ЃгыHgI42ЃЕФЮШЖЈадЧПШѕЃЌВЂДгдЊЫиЕчИКадЕФНЧЖШМгвдНтЪЭЁЃ
Д№ЃКHgCl42ЃБШHgI42ЃИќ ЃЈЬюЁАЮШЖЈЁБЛђЁАВЛЮШЖЈЁБЃЉЃЌвђЮЊ ЁЃ
ЃЈУППе3ЗжЙВМЦ21ЗжЃЉ
ФГбЇЯАаЁзщгУЭМЪОзАжУВтЖЈТСУОКЯН№жаТСЕФжЪСПЗжЪ§КЭТСЕФЯрЖддзгжЪСПЁЃ
ЃЈ1ЃЉAжаЪдМСЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЃЈ2ЃЉЪЕбщЧАЃЌЯШНЋТСУОКЯН№дкЯЁЫсжаНўХнЦЌПЬЃЌЦфФПЕФЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЃЈ3ЃЉМьВщЦјУмадЃЌНЋвЉЦЗКЭЫЎзАШыИївЧЦїжаЃЌСЌНгКУзАжУКѓЃЌашНјааЕФВйзїЛЙгаЃКЂйМЧТМCЕФвКУцЮЛжУЃЛЂкНЋBжаЪЃгрЙЬЬхЙ§ТЫЃЌЯДЕгЃЌИЩдяЃЌГЦжиЃЛЂлД§BжаВЛдйгаЦјЬхВњЩњВЂЛжИДжСЪвЮТКѓЃЌМЧТМCЕФвКУцЮЛжУЃЛЂмгЩAЯђBЕЮМгзуСПЪдМСЃЛЂнМьВщЦјУмадЁЃЩЯЪіВйзїЕФЫГађЪЧЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЈЬюађКХЃЉЃЛМЧТМCЕФвКУцЮЛжУЪБЃЌГ§ЪгЯпЦНЪгЭтЃЌЛЙгІЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЃЈ4ЃЉBжаЗЂЩњЗДгІЕФЛЏбЇЗНГЬЪНЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁ
ЃЈ5ЃЉШєЪЕбщгУТСУОКЯН№ЕФжЪСПЮЊa gЃЌВтЕУЧтЦјЬхЛ§ЮЊb mL(вбЛЛЫуЮЊБъзМзДПі)ЃЌBжаЪЃгрЙЬЬхЕФжЪСПЮЊc gЃЌдђТСЕФЯрЖддзгжЪСПЮЊЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃ
ЃЈ6ЃЉЪЕбщЙ§ГЬжаЃЌШєЮДЯДЕгЙ§ТЫЫљЕУЕФВЛШмЮяЃЌдђВтЕУТСЕФжЪСПЗжЪ§НЋЁЁЁЁЁЁЁЁЁЁЁЁЁЁЃЈЬюЁАЦЋДѓЁБЁАЦЋаЁЁБЛђЁАВЛЪмгАЯьЁБЃЉЁЃ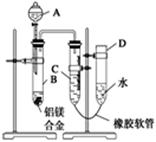
АйЖШжТаХ - СЗЯАВсСаБэ - ЪдЬтСаБэ
КўББЪЁЛЅСЊЭјЮЅЗЈКЭВЛСМаХЯЂОйБЈЦНЬЈ | ЭјЩЯгаКІаХЯЂОйБЈзЈЧј | ЕчаХеЉЦОйБЈзЈЧј | ЩцРњЪЗащЮожївхгаКІаХЯЂОйБЈзЈЧј | ЩцЦѓЧжШЈОйБЈзЈЧј
ЮЅЗЈКЭВЛСМаХЯЂОйБЈЕчЛАЃК027-86699610 ОйБЈгЪЯфЃК58377363@163.com