
题目列表(包括答案和解析)
(14分)(1)向1 L AlCl3和FeCl3混合溶液中加入含a mol NaOH的溶液时,产生的沉淀量可达最大值;继续加入NaOH溶液,沉淀开始溶解,当前后加入的NaOH总量达到b mol时,沉淀不再减少,则原溶液中Fe3+的物质的量浓度为 ,AlCl3的物质的量 。
(2)已知:2Fe3++2I- = 2Fe2++ I2; 2Fe2++Br2 = 2Fe3++2Br-
①向含有1mol FeI2和1.5mol FeBr2的溶液中通入2mol Cl2,此时被氧化的离子是 。
②如果向①的溶液中通入3mol Cl2,则被氧化的离子对应的氧化产物分别是 。
(3)①若m g铁屑与含有 n gHNO3的硝酸溶液恰好完全反应,若 m : n =" 1" : 2.7, 该反应的化学方程式为 __________________________________________________(假设还原产物只有一种,且只生成一种盐)
②若含 n g HNO3的稀硝酸溶液恰好使5.6g铁粉完全溶解,若有 n/4 gHNO3被还原成NO(无其它还原产物)则 n 的范围为_________________________
③某条件下锌和硝酸反应时的物质的量之比为2:5,此时硝酸的还原产物是____________
(14分)(1)向1 L AlCl3和FeCl3混合溶液中加入含a mol NaOH的溶液时,产生的沉淀量可达最大值;继续加入NaOH溶液,沉淀开始溶解,当前后加入的NaOH总量达到b mol时,沉淀不再减少,则原溶液中Fe3+的物质的量浓度为 ,AlCl3的物质的量 。
(2)已知:2Fe3++2I- = 2Fe2++ I2; 2Fe2++Br2 = 2Fe3++2Br-
①向含有1mol FeI2和1.5mol FeBr2的溶液中通入2mol Cl2,此时被氧化的离子是 。
②如果向①的溶液中通入3mol Cl2,则被氧化的离子对应的氧化产物分别是 。
(3)①若m g铁屑与含有 n gHNO3的硝酸溶液恰好完全反应,若 m : n =" 1" : 2.7, 该反应的化学方程式为 __________________________________________________(假设还原产物只有一种,且只生成一种盐)
②若含 n g HNO3的稀硝酸溶液恰好使5.6g铁粉完全溶解,若有 n/4 gHNO3被还原成NO(无其它还原产物)则 n 的范围为_________________________
③某条件下锌和硝酸反应时的物质的量之比为2:5,此时硝酸的还原产物是____________
(每空2分,共14分)某河道两旁有甲乙两厂。它们排放的工业废水中,共含K+、Ag+、Fe3+、C1-、OH- 、NO3- 六种离子。
甲厂的废水明显呈碱性,故甲厂废水中所含的三种离子是_____________。乙厂的废水中含有另外三种离子。对于该两厂的废水,可采取下列两种方法来处理。
(1)如果在废水中加一定量 (选填:活性炭或铁粉),可以发生反应,离子方程式是 ,并且能够回收其中的金属 (填写金属元素符号)。
(2)将甲厂和乙厂的废水按适当的比例混合,可以使废水中的某些离子转化为沉淀,写出两个离子方程式: ; 。经过滤后的废水主要含 ,可用来浇灌农田。
(14分)硫酸锌可作为食品锌强化剂的原料。工业上常用菱锌矿生产硫酸锌,菱锌矿的主要成分是ZnCO3,并含少量的Fe2O3 、FeCO3 MgO、CaO等,生产工艺流程示意如下:
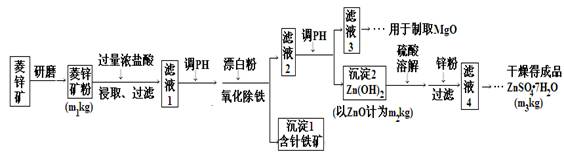
(1)将菱锌矿研磨成粉的目的是 。
(2)完成“氧化除铁”步骤中反应的离子方程式:
□Fe(OH)2+□____+□_____==□Fe(OH)3 +□Cl-
(3)针铁矿(Goethite)是以德国诗人歌德(Goethe)名字命名的,组成元素是Fe、O和H,相对分子质量为89,化学式是______。
(4)根据下表数据,调节“滤液2”的pH时,理论上可选用的最大区间为______。
|
|
Mg(OH)2 |
Zn(OH)2 |
MgCO3 |
CaCO3 |
|
开始沉淀的pH |
10.4 |
6.4 |
— |
— |
|
沉淀完全的pH |
12.4 |
8.0 |
— |
— |
|
开始溶解的pH |
— |
10.5 |
— |
— |
|
Ksp |
5.6× |
— |
6.8× |
2.8× |
(5)工业上从“滤液3”制取MgO过程中,最合适的反应物是______(选填序号)。
a.大理石粉 b.石灰乳 c.纯碱溶液 d.烧碱溶液
(6)“滤液4”之后的操作依次为______、______、过滤,洗涤,干燥。
(7)分析图中数据,菱锌矿粉中ZnCO3 的质量分数不低于________。
(14分)某探究小组的同学设计实验探究铁与水蒸气的反应,并探究反应后生成物的一系列性质。

(1)右图为铁与水蒸气反应的实验装置,实验前应先进行的操作是________________
________________ __。
(2)图I为产生水蒸气的装置,图II为铁与水蒸气反应的装置,写出硬质玻璃管B内所发生反应的化学方程式______ ________________________________。
(3)为了验证硬质玻璃管B中反应后的气体产物是H2,还需从下图中选择必要的仪器和药品,设计出一套装置,其连接顺序为:a连_______,_______连_______,_______连________。(填下列装置的接口字母)

(4)反应后,将图II装置中硬质玻璃管B内的全部固体置于试管中,加入60mL1mol/L的稀盐酸,固体恰好完全溶解,再滴加KSCN溶液,发现溶液不显血红色,写出此过程中所有可能发生反应的离子方程式__________ __、_________________________、________________________。反应前硬质玻璃管B中加入Fe粉的质量为__________g.
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com