
题目列表(包括答案和解析)
碳化硅(SiC) 、氧化铝(Al2O3) 和氮化硅(Si3N4)是优良的高温结构陶瓷,在工业生产和科技领域有重要用途。宇宙火箭和导弹中,大量用钛代替钢铁。
(1)Al的离子结构示意图为 ;
Al与NaOH溶液反应的离子方程式为
(2)氮化硅抗腐蚀能力很强,但易被氢氟酸腐蚀,氮化硅与氢氟酸反应生成四氟化硅和一种铵盐,
其反应方程式为
(3)工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g) + x N2(g) + 6 H2(g)  Si3N4(s) + 12 HCl(g) △H<0
Si3N4(s) + 12 HCl(g) △H<0
在恒温、恒容时,分别将0.3mol SiCl4(g)、0.2mol N2(g)、0.6mol H2(g)充入2 L密闭容器内,进行上述反应,5 min达到平衡状态,所得HCl(g)为0.3mol/L、 N2为0.05 mol/L
① H2的平均反应速率是
② 反应前与达到平衡时容器内的压强之比=
③ 系数 x =
(4)已知:TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g) ΔH1=+140 kJ·mol-1
C(s)+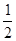 O2(g)=== CO(g) ΔH2 =-110 kJ·mol-1
O2(g)=== CO(g) ΔH2 =-110 kJ·mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式:
。
碳化硅(SiC) 、氧化铝(Al2O3) 和氮化硅(Si3N4)是优良的高温结构陶瓷,在工业生产和科技领域有重要用途。宇宙火箭和导弹中,大量用钛代替钢铁。
(1)Al的离子结构示意图为 ;
Al与NaOH溶液反应的离子方程式为
(2)氮化硅抗腐蚀能力很强,但易被氢氟酸腐蚀,氮化硅与氢氟酸反应生成四氟化硅和一种铵盐,
其反应方程式为
(3)工业上用化学气相沉积法制备氮化硅,其反应如下:
3SiCl4(g) + x N2(g) + 6 H2(g)  Si3N4(s) + 12
HCl(g) △H<0
Si3N4(s) + 12
HCl(g) △H<0
在恒温、恒容时,分别将0.3mol SiCl4(g)、0.2mol N2(g)、0.6mol H2(g)充入2 L密闭容器内,进行上述反应,5 min达到平衡状态,所得HCl(g)为0.3mol/L、 N2为0.05 mol/L
① H2的平均反应速率是
② 反应前与达到平衡时容器内的压强之比=
③ 系数 x =
(4)已知:TiO2(s)+2Cl2(g)===TiCl4(l)+O2(g) ΔH1=+140 kJ·mol-1
C(s)+ O2(g)===
CO(g) ΔH2 =-110
kJ·mol-1
O2(g)===
CO(g) ΔH2 =-110
kJ·mol-1
写出TiO2和焦炭、氯气反应生成TiCl4和CO气体的热化学方程式:
。
(8分)江苏连云港开发硅产业比较发达,粗硅提纯经常用“三氯氢硅法”。将干燥的硅粉加入合成炉中,与通入的干燥氯化氢气体在280~330℃有氯化亚铜催化剂存在下进行氯化反应,反应气体旋风分离除去杂质,再用氯化钙冷冻盐水将气态三氯氢硅冷凝成液体,经粗馏塔蒸馏和冷凝,除去高沸物和低沸物,再经精馏塔蒸馏和冷凝,得到精制三氯氢硅液体。纯度达到七个“9”以上,杂质含量小于1×10-7,硼要求在0.5×10-9以下。提纯后的三氯氢硅送入不锈钢制的还原炉内,用超纯氢气作还原剂,在1050~1100℃还原成硅,并以硅芯棒为载体沉积而得多晶硅成品。其反应式如下:
Ⅰ H2+Cl2 =" 2HCl"
Ⅱ Si(粗)+3HCl(g)= SiHCl3(l)+H2(g)
Ⅲ SiHCl3(l) +H2(g) = Si(纯)+3HCl(g)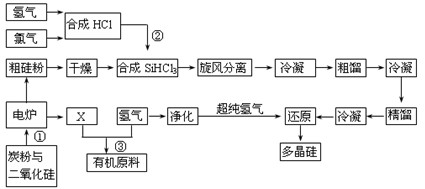
据以上材料回答问题:
(1)电炉中发生反应后排出气体X的成份 (填化学式)。
(2)目前提倡“低碳类经济”,CO2的吸收转化成有机物可有效实现碳循环,是节能减排的有效措施。某物质y的核磁共振氢谱只有一个峰,与CO2可催化加聚生成自然降解的
塑料聚碳酸酯,其反应方程式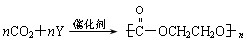 则Y的结构简式为 。
则Y的结构简式为 。
(3)在上述流程中可以循环使用的物质是 。(填名称)
(4)SiH4化学性质比较活泼,它在空气中自燃,有强还原性,在碱存在下迅速水解,由SiH4为原料进行氮化来制备Si3N4纳米材料,则你认为该材料中最大可能存在的杂质
(填化学式)。
(5)已知化学键如表
则下述反应 SiCl4(g)+2H2(g) Si(s)+4HCl(g)
Si(s)+4HCl(g)
该反应的反应热 △H= kJ·mol-1
江苏连云港开发硅产业比较发达,粗硅提纯经常用“三氯氢硅法”。将干燥的硅粉加入合成炉中,与通入的干燥氯化氢气体在280~330℃有氯化亚铜催化剂存在下进行氯化反应,反应气体旋风分离除去杂质,再用氯化钙冷冻盐水将气态三氯氢硅冷凝成液体,经粗馏塔蒸馏和冷凝,除去高沸物和低沸物,再经精馏塔蒸馏和冷凝,得到精制三氯氢硅液体。纯度达到七个“9”以上,杂质含量小于1×10-7,硼要求在0.5×10-9以下。提纯后的三氯氢硅送入不锈钢制的还原炉内,用超纯氢气作还原剂,在1050~1100℃还原成硅,并以硅芯棒为载体沉积而得多晶硅成品。其反应式如下:
Ⅰ H2+Cl2 = 2HCl
Ⅱ Si(粗)+3HCl(g)= SiHCl3(l)+H2(g)
Ⅲ SiHCl3(l) +H2(g) = Si(纯)+3HCl(g)
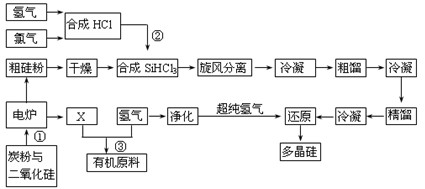
据以上材料回答问题:
(1)电炉中发生反应后排出气体X的成份 (填化学式)。
(2)目前提倡“低碳类经济”,CO2的吸收转化成有机物可有效实现碳循环,是节能减排的有效措施。某物质y的核磁共振氢谱只有一个峰,与CO2可催化加聚生成自然降解的
塑料聚碳酸酯,其反应方程式![]() 则Y的结构简式为 。
则Y的结构简式为 。
(3)在上述流程中可以循环使用的物质是 。(填名称)
(4)SiH4化学性质比较活泼,它在空气中自燃,有强还原性,在碱存在下迅速水解,由SiH4为原料进行氮化来制备Si3N4纳米材料,则你认为该材料中最大可能存在的杂质
(填化学式)。
(5)已知化学键如表

则下述反应 SiCl4(g)+2H2(g)![]() Si(s)+4HCl(g)
Si(s)+4HCl(g)
该反应的反应热 △H= kJ·mol-1
(05年江苏卷)氮化铝(AlN)具有耐高温、抗冲击、导热性好等优良性质,被广泛应用于电子工业、陶瓷工业等领域。在一定条件下,氮化铝可通过如下反应合成:()
Al2O3+N2+3C![]() 2AlN+3CO,下列叙述正确的是
2AlN+3CO,下列叙述正确的是
A 在氮化铝的合成反应中,N2是还原剂,Al2O3是氧化剂
B 上述反应中每生成2mol AlN,N2得到3mol电子
C 氮化铝中氮元素的化合价为-3价
D 氮化铝晶体属于分子晶体
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com