
题目列表(包括答案和解析)
(8分)请选择合适方法的字母代号填空:
(1)从煤焦油中提取二甲苯________;
(2)从海水中提取粗盐________;
(3)十六烷转变为辛烷和辛烯________;
(4)轻柴油转变为乙烯、丙烯等不饱和烃________;
(5)煤转化为焦炭、煤焦油等________;
(6)工业上由氧化铝制取金属铝________;
(7)从铁矿石中提取金属铁________;
(8)提纯氢氧化铁胶体(除去其中的杂质离子)________。
A.过滤 B.裂解 C.分馏 D.裂化 E.干馏 F.还原 G.电解 H.溶解
I.渗析 J.蒸发 K.氧化
(本题共8分)
(1)化学平衡常数K表示可逆反应的进行程度,K值越大,表示_________________,
K值大小与温度的关系是:温度升高,K值______________
(填一定增大、一定减小、或可能增大也可能减小)。
(2)在一体积为10L的容器中,通人一定量的CO和H2O,在850℃时发生如下反应:
CO(g)十H2O(g)  CO2(g)十H2 (g)十Q(Q>0)
CO2(g)十H2 (g)十Q(Q>0)
CO和H2O浓度变化如下图,则 0—4min的平均反应速率v(CO)=______ mol/(L·min)

(3)t℃(高于850℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如上表。
①表中3min—4min之间反应处于_________状态; C1数值_________0.08 mol/L (填大于、小于或等于)。
②反应在4min—5min问,平衡向逆方向移动,可能的原因是________(单选),表中5min—6min之间数值发生变化,可能的原因是__________(单选)。
a.增加水蒸气 b.降低温度
c.使用催化剂 d.增加氢气浓度
(13分)在所给反应条件下,有下列转化关系
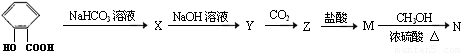
(1)推断下列各步反应所得有机物的结构简式:(每空1分,共5分)
X ;Y ;Z ;M ; N ;
(2)写出下列反应的方程式(每个方程式2分,共8分)
① X → Y
② Y → Z
③ Z → M
④ M → N
(8分)(1)在调水工程中,沿途工业污水的任意排放是造成水质恶化的最大原因。经检测某工厂废液中含有大量Mg2+、Al3+、Ag+,Fe3+、Ba2+。试分析回答下列问题:
①该废液中可能大量存在的一种阴离子是____(填序号)。
A.SO B.NO C.Cl- D.CO
②为了充分利用资源和保护环境,今要回收废液中的金属银,请你设计一个回收实验方案,并写出有关离子反应方程式: ____________________________________________
________________________________________________________________________。
(2)节能减排是中国政府报告中的关键词。火力发电厂为了减少二氧化硫的排放,往往对煤炭进行脱硫处理,而脱硫的方法有多种,下面是一种常用的脱硫方法:
微生物脱硫技术:煤炭中的硫是以FeS2存在的,在水和空气存在的条件下,脱硫微生物起生物催化作用:
①2FeS2+7O2+2H2O  4H++2Fe2++4SO42—;
4H++2Fe2++4SO42—;
②4Fe2++O2+4H+ 4Fe3++2H2O;
4Fe3++2H2O;
③FeS2+2Fe3+ 3Fe2++2S;
3Fe2++2S;
④2S+3O2+2H2O 4H++2SO42—。
4H++2SO42—。
在微生物脱硫的反应中,FeS2最终被________氧化,转化为________(填化学式)而除去;反应③中若生成0.2 mol S,则转移的电子为________mol。
(8分)某学生利用以下装置探究氯气与氨气之间的反应。其中A、F分别为氨气和氯气的发生装置,C为纯净干燥的氯气与氨气反应的装置。
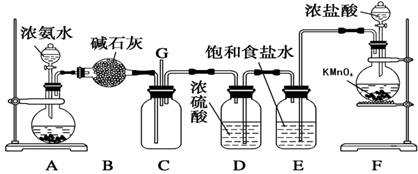
请回答下列问题:
(1)装置F中发生反应的离子方程式为_________________________。(提示,高锰酸钾的还原产物为Mn2+)
(2) B装置的名称是__________;A装置中的固体可能是________。
(3)通入C装置的两根导管左边较长、右边较短,目的是__________________。
(4)装置C内出现浓厚的白烟并在容器内壁凝结,另一生成物是空气的主要成分之一。请写出反应的化学方程式:________________________
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com