
ΧβΡΩΝ–±μ(Αϋά®¥πΑΗΚΆΫβΈω)
Θ®ΟΩΩ’2Ζ÷Θ§Ι≤30Ζ÷Θ©άϊ”ΟΓΑΜ·―ßΦΤΝΩ‘Ύ Β―ι÷–ΒΡ”Π”ΟΓ±ΒΡœύΙΊ÷Σ ΕΫχ––ΧνΩ’
Θ®1Θ©0.2 mol NH3ΤχΧε÷–Κ§ΒΡNH3Ζ÷Ή” ΐ « Θ§Τδ÷–Κ§«β‘≠Ή” ΐ « Θ§Κ§”–ΒγΉ”ΒΡΈο÷ ΒΡΝΩ « .
Θ®2Θ©1ΡΠΕϊBa(OH)2ΙΧΧε÷–Κ§”–ΒΡBa2+ΒΡΗω ΐ « Θ§»Ϊ≤Ω»ή”ΎΥ°Θ§Βγάκ≤ζ…ζΒΡOH-ΒΡΈο÷ ΒΡΝΩ « molΘ§Ά®»κΕΰ―θΜ·ΧΦΤχΧεΘ§«ΓΚΟΆξ»ΪΖ¥”ΠΘ§œϊΚΡΒΡΕΰ―θΜ·ΧΦΒΡΈο÷ ΒΡΝΩ « ΡΠΕϊΓΘ
(3)H2SO4ΒΡΡΠΕϊ÷ ΝΩ « Θ§49gH2SO4÷–Κ§”– mol―θ‘≠Ή”Θ§Κ§”–«βΒΡ÷ ΝΩ « ΓΘ
Ρή”κ ΡΠΕϊNaOH«ΓΚΟΆξ»ΪΖ¥”ΠΘ§…ζ≥…Υ°ΒΡ÷ ΝΩ « ΩΥΓΘ
(4)Κ§”–6.02ΓΝ1023Ηω―θ‘≠Ή”ΒΡH3pO4ΒΡΈο÷ ΒΡΝΩ «_________?
(5)”κ±ξΉΦΉ¥Ωωœ¬VLCO2ΥυΚ§―θ‘≠Ή” ΐΡΩœύΆ§ΒΡΥ°ΒΡ÷ ΝΩ «________(”ΟΖ÷ Ϋ±μ Ψ)
(6)ΫΪ4 g NaOH»ήΫβ‘Ύ10 mLΥ°÷–Θ§‘ΌœΓ Ά≥…1 LΘ§¥”÷–»Γ≥ω10 mLΘ§’β10 mL»ή“Κ
ΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣ__________________
(7)‘Ύ“ΜΕ®ΒΡΈ¬Ε»ΚΆ―Ι«Ωœ¬Θ§1ΧεΜΐX2 (g)Ηζ3ΧεΜΐY2 (g)Μ·Κœ…ζ≥…2ΧεΜΐΜ·ΚœΈοΘ§‘ρΗΟΜ·ΚœΈοΒΡΜ·―ß Ϋ «_______________
Θ®ΟΩΩ’2Ζ÷Θ§Ι≤30Ζ÷Θ©άϊ”ΟΓΑΜ·―ßΦΤΝΩ‘Ύ Β―ι÷–ΒΡ”Π”ΟΓ±ΒΡœύΙΊ÷Σ ΕΫχ––ΧνΩ’
Θ®1Θ©0.2mol NH3ΤχΧε÷–Κ§ΒΡNH3Ζ÷Ή” ΐ « Θ§Τδ÷–Κ§«β‘≠Ή” ΐ « Θ§Κ§”–ΒγΉ”ΒΡΈο÷ ΒΡΝΩ « .
Θ®2Θ©1ΡΠΕϊBa(OH)2ΙΧΧε÷–Κ§”–ΒΡBa2+ΒΡΗω ΐ « Θ§»Ϊ≤Ω»ή”ΎΥ°Θ§Βγάκ≤ζ…ζΒΡOH-ΒΡΈο÷ ΒΡΝΩ « molΘ§Ά®»κΕΰ―θΜ·ΧΦΤχΧεΘ§«ΓΚΟΆξ»ΪΖ¥”ΠΘ§œϊΚΡΒΡΕΰ―θΜ·ΧΦΒΡΈο÷ ΒΡΝΩ « ΡΠΕϊΓΘ
(3)H2SO4ΒΡΡΠΕϊ÷ ΝΩ « Θ§49gH2SO4÷–Κ§”– mol―θ‘≠Ή”Θ§Κ§”–«βΒΡ÷ ΝΩ « ΓΘ
Ρή”κ ΡΠΕϊNaOH«ΓΚΟΆξ»ΪΖ¥”ΠΘ§…ζ≥…Υ°ΒΡ÷ ΝΩ « ΩΥΓΘ
(4)Κ§”–6.02ΓΝ1023Ηω―θ‘≠Ή”ΒΡH3pO4ΒΡΈο÷ ΒΡΝΩ «_________?
(5)”κ±ξΉΦΉ¥Ωωœ¬VLCO2ΥυΚ§―θ‘≠Ή” ΐΡΩœύΆ§ΒΡΥ°ΒΡ÷ ΝΩ «________(”ΟΖ÷ Ϋ±μ Ψ)
(6)ΫΪ4 g NaOH»ήΫβ‘Ύ10 mLΥ°÷–Θ§‘ΌœΓ Ά≥…1 LΘ§¥”÷–»Γ≥ω10 mLΘ§’β10mL»ή“Κ
ΒΡΈο÷ ΒΡΝΩ≈®Ε»ΈΣ__________________
(7)‘Ύ“ΜΕ®ΒΡΈ¬Ε»ΚΆ―Ι«Ωœ¬Θ§1ΧεΜΐX2(g)Ηζ3ΧεΜΐY2 (g)Μ·Κœ…ζ≥…2ΧεΜΐΜ·ΚœΈοΘ§‘ρΗΟΜ·ΚœΈοΒΡΜ·―ß Ϋ «_______________
 ΓΘ
ΓΘ(ΟΩΩ’1Ζ÷,Ι≤7Ζ÷)‘ΎΜ·―ßΖ¥”Π÷–Θ§÷Μ”–ΦΪ…Ό ΐΡήΝΩ±»ΤΫΨυΡήΝΩΗΏΒΟΕύΒΡΖ¥”ΠΈοΖ÷Ή”ΖΔ…ζ≈ωΉ≤ ±≤≈Ω…ΡήΖΔ…ζΜ·―ßΖ¥”ΠΘ§’β–©Ζ÷Ή”±Μ≥ΤΈΣΜνΜ·Ζ÷Ή”ΓΘ ΙΤ’Ά®Ζ÷Ή”±δ≥…ΜνΜ·Ζ÷Ή”Υυ–ηΧαΙ©ΒΡΉνΒΆœόΕ»ΒΡΡήΝΩΫ–ΜνΜ·ΡήΘ§ΤδΒΞΈΜΆ®≥Θ”ΟkJΓΛmolΘ≠1±μ ΨΓΘ«κ»œ’φΙέ≤λœ¬ΆΦΘ§»ΜΚσΜΊ¥πΈ ΧβΓΘ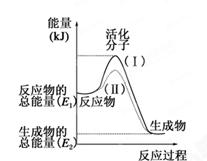
Θ®1Θ©ΆΦ÷–Υυ ΨΖ¥”Π «________(ΧνΓΑΈϋ»»Γ±ΜρΓΑΖ≈»»Γ±)Ζ¥”ΠΓΘ
Θ®2Θ©“―÷Σ≤πΩΣ1mol HΓΣHΦϋΓΔ1mol IΓΣIΓΔ1mol HΓΣIΦϋΖ÷±π–η“ΣΈϋ ’ΒΡΡήΝΩΈΣ436kJΓΔ151kJΓΔ299kJΓΘ‘ρ”…1mol«βΤχΚΆ1mol ΒβΖ¥”Π…ζ≥…HIΜα________(ΧνΓΑΖ≈≥ωΓ±ΜρΓΑΈϋ ’Γ±)________kJΒΡ»»ΝΩΓΘ‘ΎΜ·―ßΖ¥”ΠΙΐ≥Χ÷–Θ§ «ΫΪ______ΉΣΜ·ΈΣ________ΓΘ
Θ®3Θ©œ¬Ν–Ζ¥”Π÷–Θ§ τ”ΎΖ≈»»Ζ¥”ΠΒΡ «________Θ§ τ”ΎΈϋ»»Ζ¥”ΠΒΡ «________ΓΘ
ΔΌΈο÷ »Φ…’ ΔΎ’®“©±§’® ΔέΥαΦν÷–ΚΆΖ¥”Π ΔήΕΰ―θΜ·ΧΦΆ®Ιΐ≥ψ»»ΒΡΧΦ
Δί ≥Έο“ρ―θΜ·ΕχΗ·Αή ΔόBa(OH)2ΓΛ8H2O”κNH4ClΖ¥”Π ΔΏΧζΖέ”κœΓ―ΈΥαΖ¥”Π
Θ®10Ζ÷Θ§ΟΩΩ’2Ζ÷Θ©Θ®1Θ©œ¬Ν–Ζ¥”Π÷– τ”Ύ―θΜ·ΜΙ‘≠Ζ¥”ΠΒΡ « ΓΘΘ®Χν–ρΚ≈Θ©
A. MnO2 + 4HClΘ®≈®Θ©= MnCl2 + Cl2Γϋ+ 2H2O B.SO2+2H2S = 2H2O+3SΓΐ
CΘ°Ba(OH)2 + H2SO4 =BaSO4Γΐ+2H2O DΘ°Cl2+2NaOH= NaCl +NaClO+H2O
Θ®2Θ©“―÷ΣKMnO4 ”κ≈®―ΈΥαΖΔ…ζ»γœ¬Ζ¥”ΠΘΚ
2KMnO4 + 16HCl(≈®)=== 2KCl + 2MnCl2 + 5Cl2Γϋ+8H2OΓΘ
‘Ύ…œ ωΖ¥”Π÷–Θ§―θΜ·ΦΝ « ΓΘ”ΟΒΞœΏ«≈Ζ®±ξ≥ω¥ΥΖ¥”ΠΒΡΒγΉ”ΉΣ“ΤΖΫœρΚΆ ΐΡΩΓΘ
Θ®3Θ©”–œ¬Ν–6÷÷Έο÷ ΘΚK2SO4ΓΔK2SO3ΓΔI2ΓΔH2SO4ΓΔKIO3ΓΔH2OΉι≥…“ΜΗω―θΜ·ΜΙ‘≠Ζ¥”ΠΘ§“―÷Σ‘ΎΖ¥”Π÷–K2SO3 ß»ΞΒγΉ”ΓΘ«κΜΊ¥πœ¬Ν–Έ ΧβΘΚ
ΔΌΫΪ’β6÷÷Έο÷ Ζ÷±πΧν»κœ¬ΟφΕ‘”ΠΒΡΚαœΏ…œΘ§Ήι≥…“ΜΗωΈ¥≈δΤΫΒΡΜ·―ßΖΫ≥Χ ΫΘΚ
________ΘΪ________ΘΪH2SO4Γζ ________ΘΪ________ΘΪ________Θ®ΧνΜ·―ß ΫΘ©
ΔΎΖ¥”Π÷–1mol―θΜ·ΦΝΒΟΒΫ______molΒγΉ”ΓΘ
ΑΌΕ»÷¬–≈ - ΝΖœΑ≤αΝ–±μ - ‘ΧβΝ–±μ
Κΰ±± ΓΜΞΝΣΆχΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΤΫΧ® | Άχ…œ”–ΚΠ–≈œΔΨΌ±®Ή®«χ | Βγ–≈’©Τ≠ΨΌ±®Ή®«χ | …φάζ Ζ–ιΈό÷ς“ε”–ΚΠ–≈œΔΨΌ±®Ή®«χ | …φΤσ«÷»®ΨΌ±®Ή®«χ
ΈΞΖ®ΚΆ≤ΜΝΦ–≈œΔΨΌ±®ΒγΜΑΘΚ027-86699610 ΨΌ±®” œδΘΚ58377363@163.com