
题目列表(包括答案和解析)
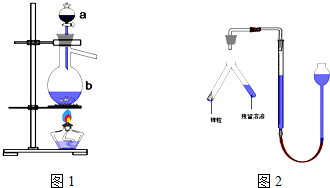
A.V=20 B.20<V<40
C.V=40 D.V>40
设NA为阿伏加德罗常数的值,下列说法中正确的是
A.标准状况下,22.4 L三氯甲烷中共价键数目为4NA
B.1mol Na2O2与足量的CO2和H2O(g)的混合物反应,转移的电子数为NA
C.足量MnO2与含4 mol HCl的浓盐酸反应生成的Cl2分子数为NA
D.1mol Cl2溶于水中转移的电子数为NA
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com