
题目列表(包括答案和解析)
下列说法正确的是 ( )
①用25mL酸式滴定管可以准确放出8.00mL的稀盐酸;
②可用干燥的pH试纸测定氯水的pH;
③使用容量瓶配制溶液,定容时俯视,所得溶液的浓度偏大;
④加入盐酸有使澄清石灰水变浑浊的无色气体生成,则原溶液中一 定有大量CO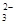 存在;
存在;
⑤在某温度下,醋酸与氢氧化钠溶液混合,溶液呈碱性,溶液中离子浓度大小的关系一定为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+);
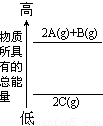
⑥右图是反应物和生成物的能量示意图,其可能发生反应的热化学方程式:2A(g)+B(g) 2C(g) △H=QkJ·mol-1(Q<0)
2C(g) △H=QkJ·mol-1(Q<0)
A.①③⑥ B.②④⑤ C.①③④ D.③⑤⑥
下列说法正确的是
①用25 mL酸式滴定管可以准确放出8.00 mL的稀盐酸;
②可用干燥的pH试纸测定氯水的pH;
③使用容量瓶配制溶液,定容时俯视,所得溶液的浓度偏大;
④加入盐酸有能使澄清石灰水变浑浊的无色气体生成,则原溶液中—定有大量CO32-存在;
⑤在某温度下,一定量的醋酸与氢氧化钠溶液充分混合,若溶液呈碱性时,溶液中离子浓度大小的关系一定为: c(Na+)﹥c(CH3COO—)﹥c(OH—)﹥c(H+);
⑥下图是反应物和生成物的能量变化示意图,其可能发生反应的热化学方程式可表示为:2 A(g)+ B(g) = 2 C(g);△H=Q kJ·mol-1(Q<0 )。

A.①③⑥ B.②④⑤
C.①③④ D.③⑤⑥
下列说法正确的是( )
| A.在中和热的测定实验中,将氢氧化钠溶液迅速倒入盛有盐酸的量热计中,立即读出并记录溶液的起始温度 |
B.如图,一段时间后给烧杯内地溶液中加入黄色的 溶液,可看到Fe电极附近有蓝色沉淀生成 溶液,可看到Fe电极附近有蓝色沉淀生成 |
| C.用标准盐酸滴定待测NaOH溶液,水洗后的酸式滴定管未经标准液润洗,则测定结果偏低 |
D.用加热的方式可提取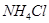 固体中混有的少量的碘 固体中混有的少量的碘 |



 Y 的进程图解。图中的“
Y 的进程图解。图中的“ ”是X,“
”是X,“ ”是Y 则可以计算得到乙的平衡常数K=1,且比甲的平衡常数要小
”是Y 则可以计算得到乙的平衡常数K=1,且比甲的平衡常数要小 下列说法正确的是( )
①用25mL酸式滴定管可以准确放出8.00mL的稀盐酸;
②可用干燥的pH试纸测定氯水的pH;
③使用容量瓶配制溶液,定容时俯视,所得溶液的浓度偏大;
④加入盐酸有能使澄清石灰水变浑浊的无色气体生成,则原溶液中一定有大量CO![]() 存在;
存在;
⑤在某温度下,一定量的醋酸与氢氧化钠溶液充分混合,若溶液呈碱性时,溶液中离子浓度大小的关系一定为:c(Na+)>c(CH3COO-)>c(OH-)>c(H+);
⑥下图是反应物和生成物的能量变化示意图,其可能发生反应的热化学方程式可表示为:2A(g)+B(g) ![]() 2C(g);△H=QkJ?mol-1(Q<0)。
2C(g);△H=QkJ?mol-1(Q<0)。

A.①③⑥ B.②④⑤ C.①③④ D.③⑤⑥
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com