
题目列表(包括答案和解析)
像根瘤菌那样在常温常压下把游离氮固定下来供作物吸收,这种方法称之为生物模拟固氮。近年来,国内外科学家正在探索这一课题,纷纷把目光集中在根瘤菌上,研究具有非凡固氮功能的固氮酶的组成和结构。固氮酶由二氮酶和二氮还原酶两种蛋白质组成,含有一定数量的钼原子、铁原子和酸溶性的硫原子。由于二氮还原酶在空气中暴露30秒,活性就会丧失一半,故至今仍未搞清固氮酶的固氮机理。但使非豆科植物的根部也结出根瘤的研究却取得令人欣喜的突破。
1.氮的固定是指_______.
A.植物从土壤中吸收含氮养料
B.豆科植物根瘤菌将含氮化合物转变为植物蛋白质
C.将氨转变成硝酸及其他氮的化合物
D.将空气中的氮气转变为含氮的化合物
2.二氮酶这种蛋白质お的1%水溶液渗透压在24℃是112Pa,该蛋白质的含铁量是0.814%。 根据渗透压值,算出二氮酶的分子量(答数不满1000就舍去)__________________。
3.为确定固氮的最终产物,做了如下实验:
①把固氮菌培养在含15N2的空气中,细胞迅速固定N元素,短期内细胞的谷氨酸便出现大量的15N。
②如果把细胞培养于含有15NH3的培养基中,固氮能力立刻停止,但吸入的氨态氮迅速转入谷氨酸中。
(1)由此可推出固氮的最终产物为________。
(2)工业上固氮的方法是(写出反应条件)________。若生物固氮也是按此反应进行,你认为何者效率高?简述理由?______________________________________________________
4.某生态系统中氮循环简图如图所示:

(1)哪一类生物能将蛋白质转化为氨__________.
A.分解者
B.藻类
C.化能合成类生物
(2)该生态系统的豆科植物不施氮肥,仍能表现出良好的长势,其原因是________。
(3)雷雨中常含有微量的硝酸而为农作物所利用,用化学方程式解释HNO3的形成过程_____ __ _。
(4)硝化细菌能够将NH3氧化为硝酸和亚硝酸,写出有关的化学反应方程式_______
5.很久以前,澳大利亚有着大片大片荒芜的土地,近几十年来,他们重视对生物固氮的研究利用,培育和引进了优良的豆科牧草良种,选育了高效的和适应性强的根瘤菌,结果形成了一望无际的优良牧场。褐球固氮菌于有氧状态下,在无氮培养中生长时,通过固定空气中氮取得它所需要的氮,在标准大气压和303K时,多少体积的空气能够供应1dm3的细菌所需要的氮气,已知该细菌每立方厘米重为0.84mg,含氮量为7%,空气中N2的体积百分比为78%。
1.氮的固定是指_______.
A.植物从土壤中吸收含氮养料
B.豆科植物根瘤菌将含氮化合物转变为植物蛋白质
C.将氨转变成硝酸及其他氮的化合物
D.将空气中的氮气转变为含氮的化合物
2.二氮酶这种蛋白质お的1%水溶液渗透压在24℃是112Pa,该蛋白质的含铁量是0.814%。 根据渗透压值,算出二氮酶的分子量(答数不满1000就舍去)__________________。
3.为确定固氮的最终产物,做了如下实验:
①把固氮菌培养在含15N2的空气中,细胞迅速固定N元素,短期内细胞的谷氨酸便出现大量的15N。
②如果把细胞培养于含有15NH3的培养基中,固氮能力立刻停止,但吸入的氨态氮迅速转入谷氨酸中。
(1)由此可推出固氮的最终产物为________。
(2)工业上固氮的方法是(写出反应条件)________。若生物固氮也是按此反应进行,你认为何者效率高?简述理由?______________________________________________________
4.某生态系统中氮循环简图如图所示:

(1)哪一类生物能将蛋白质转化为氨__________.
A.分解者
B.藻类
C.化能合成类生物
(2)该生态系统的豆科植物不施氮肥,仍能表现出良好的长势,其原因是________。
(3)雷雨中常含有微量的硝酸而为农作物所利用,用化学方程式解释HNO3的形成过程_____ __ _。
(4)硝化细菌能够将NH3氧化为硝酸和亚硝酸,写出有关的化学反应方程式_______
5.很久以前,澳大利亚有着大片大片荒芜的土地,近几十年来,他们重视对生物固氮的研究利用,培育和引进了优良的豆科牧草良种,选育了高效的和适应性强的根瘤菌,结果形成了一望无际的优良牧场。褐球固氮菌于有氧状态下,在无氮培养中生长时,通过固定空气中氮取得它所需要的氮,在标准大气压和303K时,多少体积的空气能够供应1dm3的细菌所需要的氮气,已知该细菌每立方厘米重为0.84mg,含氮量为7%,空气中N2的体积百分比为78%。
 CH3OH(g)过程中 能量变化如下图。曲线Ⅱ表示使用催化剂时的能量变化。若投入amol CO、2amol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值。
CH3OH(g)过程中 能量变化如下图。曲线Ⅱ表示使用催化剂时的能量变化。若投入amol CO、2amol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值。 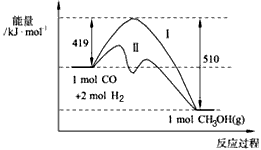
 CH3OH(g) ΔH>-91 kJ·mol-1
CH3OH(g) ΔH>-91 kJ·mol-1 
(3)氧化还原反应中实际上包含氧化和还原两个过程。下面是HNO3发生的一个还原过程的反应式:
NO3-+4H++3e-→NO+2H2O
① KMnO4、Na2CO3、CuO、KI四种物质中的______________(填化学式)能使上述还原过程发生。
②欲用上图II装置通过测定气体生成量测算硝酸被还原的速率,当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测定_________________________推算反应速率。
(18分)应用化学反应需要研究化学反应的条件、限度和速率。
![]() (1)已知反应:Br2+2Fe2+=2Br-+2Fe3+,向10 mL 0.1 mol?L-1的FeBr2溶液中通入0.001mol Cl2,反应后,溶液中除含有Cl-外,还一定 (填序号)。
(1)已知反应:Br2+2Fe2+=2Br-+2Fe3+,向10 mL 0.1 mol?L-1的FeBr2溶液中通入0.001mol Cl2,反应后,溶液中除含有Cl-外,还一定 (填序号)。
![]() ① 含Fe2+,不含Fe3+ ② 含Fe3+,不含Br- ③ 含Fe3+,含有Br-
① 含Fe2+,不含Fe3+ ② 含Fe3+,不含Br- ③ 含Fe3+,含有Br-
![]() (2)773 K,固定体积的容器中,反应CO(g)+2H2(g)
(2)773 K,固定体积的容器中,反应CO(g)+2H2(g) ![]() CH3OH(g)过程中能量变化如下图。曲线Ⅱ表示使用催化剂时的能量变化。若投入a mol CO、2a mol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值。
CH3OH(g)过程中能量变化如下图。曲线Ⅱ表示使用催化剂时的能量变化。若投入a mol CO、2a mol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值。
① 若按上述投料比使该反应具有工业应用价值,CO的平衡转化率为 ;
② 在容器容积不变的前提下,欲提高H2的转化率,可采取的措施(答两项即可) 、 ;
③ 下列与催化剂有关的说法中,正确的是 (填字母序号)。
a.使用催化剂,使反应CO(g)+2H2(g) ![]() CH3OH(g) ΔH>-91 kJ?mol-1
CH3OH(g) ΔH>-91 kJ?mol-1
b.使用催化剂,不能改变反应的平衡常数K
c.使用催化剂,能够提高反应物转化率
![]() (3)高铁酸盐在能源环保领域有广泛用途。我国学者提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如右图所示。
(3)高铁酸盐在能源环保领域有广泛用途。我国学者提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如右图所示。
① Fe电极作 极(填“阴”或“阳”);
② Ni电极的电极反应式为: 。
(4)氧化还原反应中实际上包含氧化和还原两个过程。下面是HNO3发生的一个还原过程的反应式:
NO3-+4H++3e-= NO+2H2O
①KMnO4、Na2CO3、CuO、KI四种物质中的 (填化学式)能使上述还原过程发生。
②欲用下图装置通过测定气体生成量测算硝酸被还原的速率,当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测定 推(计)算反应速率。
应用化学反应需要研究化学反应的条件、限度和速率。
(1)已知反应:Br2+2Fe2+=2Br-+2Fe3+ ,向10 mL 0.1 mol·L-1的FeBr2溶液中通入0.001 mol Cl2,反应后,溶液中除含有Cl-外,还一定有 (填序号)。
①含Fe2+,不含Fe3+② 含Fe3+,不含Br-③ 含Fe3+,还含有Br-
(2)773 K、固定体积的容器中,反应CO(g)+2H2(g)![]() CH3OH(g)过程中能量变化如下图。曲线Ⅱ表示使用催化剂时的能量变化。若投入a mol CO、2a mol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值。
CH3OH(g)过程中能量变化如下图。曲线Ⅱ表示使用催化剂时的能量变化。若投入a mol CO、2a mol H2,平衡时能生成0.1a mol CH3OH,反应就具工业应用价值。
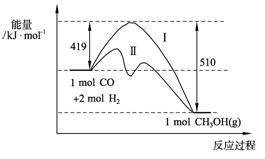
①若按上述投料比使该反应具有工业应用价值,CO的平衡转化率最小为 ;
②在容器容积不变的前提下,欲提高H2的转化率,可采取的措施(答两项即可) 、 ;
③下列与催化剂有关的说法中,正确的是 (填字母序号)。
a. 使用催化剂,使反应CO(g)+2H2(g)![]() CH3OH(g) ΔH>-91 kJ·mol-1
CH3OH(g) ΔH>-91 kJ·mol-1
b. 使用催化剂, 能够提高反应物转化率
c. 使用催化剂,不能改变反应的平衡常数K
(3)高铁酸盐在能源环保领域有广泛用途。我国学者提出用镍(Ni)、铁作电极电解浓NaOH溶液制备高铁酸盐Na2FeO4的方案,装置如右图所示。
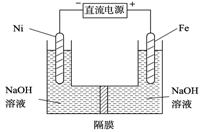
① Ni作 (填“阴”或“阳”) 极;
②Ni电极的电极反应式为: 。
(4)氧化还原反应中实际上包含氧化和还原两个过程。下面是HNO3发生的一个还原过程的反应式:NO-3+4H++3e-→NO+2H2O
①KMnO4、HCl、Fe(NO3)2、CuO、KI五种物质中的 (填化学式)能使上述还原过程发生。
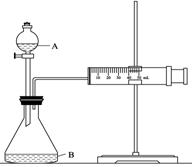
②欲用下图装置通过测定气体生成量测算硝酸被还原的速率,当反应物的浓度、用量及其他影响速率的条件确定之后,可以通过测定 推(计)算反应速率。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com