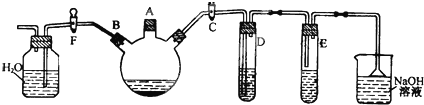
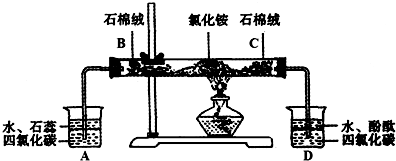
有以下实验装置可供选择:
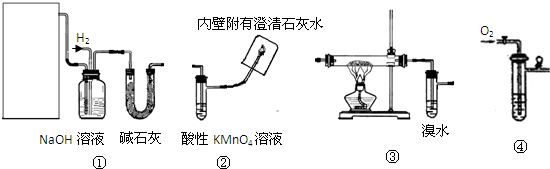
Ⅰ、实验室用甲醇催化氧化法得到甲醛,并验证甲醛的性质.请回答下列问题:
(1)应选择的装置是
③④(或④③)
③④(或④③)
(填写编号);
(2)若③硬质玻璃管中装有铜粉,请写出硬质玻璃管中发生反应的化学方程式
;
HCHO+H2O+Br2→HCOOH+2HBr
HCHO+H2O+Br2→HCOOH+2HBr
(3)实验结束后,观察到溴水褪色.为解释这一现象,某学习小组的同学提出两种猜想:
A.发生了加成反应;
B.发生了氧化反应.为探究哪种猜想正确,学习小组的同学用pH计测溴水褪色前后溶液的pH.测得溶液的pH下降,试写出褪色的化学方程式
HCHO+H2O+2Br2→CO2+4HBr
HCHO+H2O+2Br2→CO2+4HBr
Ⅱ、若选择①③②验证乙烯与氢气反应产物,请回答下列问题:
(4)写出实验室制乙烯的化学方程式
;
(5)NaOH溶液的作用是
①除去乙烯中的酸性气体,②使乙烯与氢气混合,③观察气泡并调节乙烯与氢气混合的体积之比
①除去乙烯中的酸性气体,②使乙烯与氢气混合,③观察气泡并调节乙烯与氢气混合的体积之比
;
(6)实验过程中,发现③中溴水褪色,试用化学方程式表示溴水褪色的原因
CH2=CH2+Br-Br→CH2Br-CH2Br
CH2=CH2+Br-Br→CH2Br-CH2Br
;
(7)出现什么现象可说明乙烯与氢气反应生成了乙烷
②中酸性KMnO4溶液不褪色,点燃气体后附有澄清石灰水的烧杯壁出现白色沉淀
②中酸性KMnO4溶液不褪色,点燃气体后附有澄清石灰水的烧杯壁出现白色沉淀
.