
题目列表(包括答案和解析)
(11分)电化学在工业生产中有广泛应用。
(1)右图所示装置中,两玻璃管及烧杯中是滴有酚酞的NaCl饱和溶液,
C(I)、C(II)为多孔石墨电极。

①电解NaCl饱和溶液的化学方程式为 。
②接通S1后,C(I)附近溶液变红,两玻璃管中有气体生成。则电极C(I)是 (填“阳”或“阴”) 极;检验C(II)电极反应所得气体产物的方法和现象是 。
③一段时间后(玻璃管中液面未脱离电极),断开S1,则C(I)、C(II)两玻璃管内气体的体积V(I)、V(II)的关系是:V(I) V(II)(填“>”、 “=”或 “<”) 。断开S1接通S2,电流表的指针发生偏转,此时电极C(II) 是 (填“正”或“负”) 极;C(I) 的电极反应是: 。
(2)若用此装置精炼粗铜,断开S2,接通S1,电解液选用CuSO4溶液,当电路中有0.04 mol电子通过时,阴极增重 g。
(11分)在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。

(1)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选 填字母):a接 , 接 , 接h;
用A装置制取NH3的化学反应方程式为
(2)用下图所示装置也可以制取NH3,则圆底烧瓶中的固体可以选用 (选填字母编号);

A、碱石灰 B、生石灰 C、无水氯化钙 D、无水硫酸铜 E、烧碱
(3)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙 时,应先通入的气体是 ,试写出制纳米级碳酸钙的化学方程式 ;
(4)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
(11分)电化学在工业生产中有广泛应用。
(1)右图所示装置中,两玻璃管及烧杯中是滴有酚酞的NaCl饱和溶液,
C(I)、C(II)为多孔石墨电极。
①电解NaCl饱和溶液的化学方程式为 。
②接通S1后,C(I)附近溶液变红,两玻璃管中有气体生成。则电极C(I)是 (填“阳”或“阴”) 极;检验C(II)电极反应所得气体产物的方法和现象是 。
③一段时间后(玻璃管中液面未脱离电极),断开S1,则C(I)、C(II)两玻璃管内气体的体积V(I)、V(II)的关系是:V(I) V(II)(填“>”、 “=”或 “<”) 。断开S1接通S2,电流表的指针发生偏转,此时电极C(II) 是 (填“正”或“负”) 极;C(I) 的电极反应是: 。
(2)若用此装置精炼粗铜,断开S2,接通S1,电解液选用CuSO4溶液,当电路中有0.04 mol电子通过时,阴极增重 g。
(11分)在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。
(1)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选 填字母):a接 , 接 , 接h;
用A装置制取NH3的化学反应方程式为
(2)用下图所示装置也可以制取NH3,则圆底烧瓶中的固体可以选用 (选填字母编号);
A、碱石灰 B、生石灰 C、无水氯化钙 D、无水硫酸铜 E、烧碱
(3)向浓CaCl2溶液中通入NH3和CO2气体制纳米级碳酸钙 时,应先通入的气体是 ,试写出制纳米级碳酸钙的化学方程式 ;
(4)试设计简单的实验方案,判断所得碳酸钙样品颗粒是否为纳米级
(11分)在浓CaCl2溶液中通入NH3和CO2,可以制得纳米级碳酸钙(粒子直径在1~100nm之间)。下图所示A~E为实验室常见的仪器装置(部分固定夹持装置略去),请根据要求回答问题。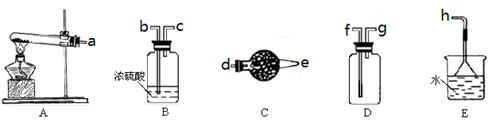
(1)实验室制取、收集干燥的NH3,需选用上述仪器装置的接口连接顺序是(选 填字母):a接 , 接 , 接h;
用A装置制取NH3的化学反应方程式为
(2)用下图所示装置也可以制取NH3,则圆底烧瓶中的固体可以选用 (选填字母编号);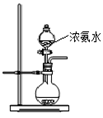
| A.碱石灰 | B.生石灰 | C.无水氯化钙 | D.无水硫酸铜 E、烧碱 |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com