
题目列表(包括答案和解析)
(7分)同学们通过查阅资料知道,过氧化氢分解反应的催化剂除二氧化锰外,还有氯化铁溶液、氯化铜溶液中的金属离子和土豆中含有的过氧化氢酶。同学们通过如下实验进行相关研究。
实验一:验证二氧化锰能加快过氧化氢的分解速率
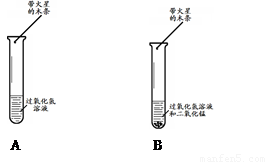
分别取5 mL 5%的过氧化氢溶液于两支试管中,向B中试管内加入少量二氧化锰(如上图所示)。A中带火星的木条不复燃,B中带火星的木条复燃,实验证明二氧化锰加快了过氧化氢的分解速率。A中木条不复燃的原因是 ,B中反应的化学方程式是 。
实验二:研究催化剂的某些因素对过氧化氢分解速率的影响
方案Ⅰ:分别取20 mL 5%的过氧化氢溶液于3个大小相同的锥形瓶中。向其中两个锥形瓶中分别加入含相同数目金属离子的氯化铁溶液和氯化铜溶液,分别连接传感器测体系压强(如右图所示)。测定数据如下表所示:

|
试剂 压强/KPa |
0 |
60 |
120 |
180 |
240 |
300 |
|
20mL 5%的过氧化氢溶液 |
101.86 |
102.99 |
103.42 |
103.67 |
103.99 |
104.00 |
|
加入氯化铁溶液 |
102.21 |
105.35 |
115.40 |
129.69 |
145.52 |
163.99 |
|
加入氯化铜溶液 |
101.50 |
102.73 |
107.53 |
114.78 |
122.49 |
130.39 |
(1)加入含相同数目金属离子的氯化铁溶液和氯化铜溶液,该步操作的实验目的是 。
(2)根据上表数据得出的结论是 。
方案Ⅱ:从同一部位取2个质量均为1.7 g的正方体土豆块,将其中一块切成若干片,片与片相连不断开,同时分别放入盛30 mL 5%过氧化氢溶液的50 mL量筒中。均看到有气泡生成,一段时间,只有土豆片不断上升。通过实验得出的结论是 。
【实验反思】通过实验一和实验二说明,测量不同的物理量可判断过氧化氢的分解速率。
下列做法中能比较过氧化氢的分解速率的是 (填选项序号)。
A. 测量完全反应后气体的总体积 B. 测量相同时间内产生气体的体积
C. 测量相同时间内体系压强的变化 D. 测量相同时间内溶液质量的变化
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com