
题目列表(包括答案和解析)
 (1)如何检查D装置的气密性?
(1)如何检查D装置的气密性?
| ||
| ||
下图实验装置示意图中A是简易的H2发生器,B是大小适宜的的圆底烧瓶,C是装有干燥剂的U形管。A是旋转活塞,D是装有还原铁粉的反应管,E是装有酚酞的试管。实验前先检查装置的气密性。实验开始时,先关闭活塞a,并取下烧瓶B;向A制加入一定量浓度适当的盐酸,产生H2。:经必要的“操作”后,在导管口处点燃H2,然后如图所示套上烧瓶B,塞紧烧瓶,H2在烧瓶中继续燃烧,用酒精灯加热反应管D中的还原铁粉,待B中H2的火焰熄灭后,打开活塞a,气体通过反应管D进入烧杯E中,使酚酞试液呈红色。
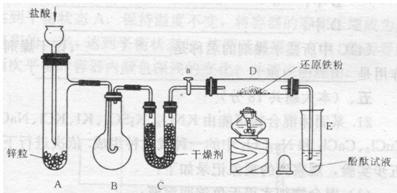
请回答下列问题。
(1)实验前如何检查整套装置的气密性? 。
(2)题干中必要操作步骤指的是
(3)操作中先加热D后打开a的目的是
(4)写出B、D中分别发生反应的化学方程式:B中 ,
D中 。
(5)C中的干燥剂的名称是 ,该干燥剂的作用是 。
现有实验药品:一定质量的锌(分片状和粒状两种)、浓H2SO4(密度1.84g·cm-3)、水以及下图装置,图中量气管B是由甲、乙两根玻璃管组成,它们有橡皮管连通,并装适量水,甲管有刻度(0~100mL),甲、乙管可固定在铁架上,供量气用,乙管可上下移动,以调节液面高低,利用此装置可测定锌的相对原子质量.(设锌全部反应,产生的气体不超过50mL)回答下列问题:

(1)实验前为检查装置的气密性,先将A,甲、乙三管固定,乙管中注入水,液面高于甲液面,静置片刻,________________________,说明装置气密性良好.
(2)按图示装置实验,要保证不漏出H2,应如何操作?___________________________.
(3)为了准确地测量H2的体积,在读取反应后甲管中液面的读数时,应注意________(填写序号).
(A)视线与凹液面最低处相平
(B)等待片刻,待乙管液面不再上升时读数
(C)读数时应上、下移动乙管,使甲、乙两管液面相平
(D)读数时不一定使甲、乙两管液面相平
(4)设计一个不用量气管,而用中学常用仪器测量H2体积的装置,应选用的仪器(自选)是_____________________________________________________________________________________________________________________________________________________.
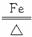
(1)实验前如何检验装置的气密性?
答:_________________________________________________________________。
(2)点燃氢气前必须进行_____________操作,该操作方法是____________________________。
(3)写出B、D中分别发生反应的化学方程式。B中____________________,D中________________。
(4)C中所盛干燥剂的名称是___________,该干燥剂的作用是___________________________。
(14分)某同学用图示装置进行铁和稀硝酸反应的实验并进行相关的实验探究。
a.向广口瓶内注入足量热NaOH溶液,将盛有一定质量的纯铁粉的小烧杯放入瓶中。
b.关闭止水夹,点燃红磷,伸人瓶中,塞好胶塞。
c.待红磷充分燃烧,一段时间后打开分液漏斗旋塞,向烧杯中缓慢滴入一定量的4mol·L-1的稀硝酸,
铁粉完全溶解。
(一)气体产物成分探究
(1)实验前如何检查该装置的气密性? 。
(2)燃烧红磷的目的是 。
(3)为证明气体产物为NO,步骤c后还缺少的一步主要操作是 。
(二)产物中铁元素价态探究:
(1)提出合理假设:
假设1:产物中只有+2价铁;假设2: ,假设3:产物中既有+2价铁,又有+3价铁。
(2)设计实验方案,验证假设1成立(写出实验操作步骤、现象和结论): 。
(三)问题讨论
(1)广口瓶中热NaOH溶液的主要作用是 。
(2)若假设3成立,且所得溶液中n(Fe2+):n(Fe3+)=3:1时,则对应的离子反应方程式为 。
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com