
题目列表(包括答案和解析)
| ||
| ||
| ||
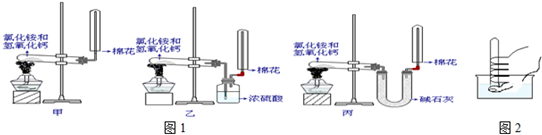
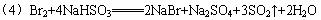
①装置如图所示,检查其气密性。
②向仪器Ⅰ中加入一定体积的水和浓H2SO4,冷却至室温。然后,向仪器Ⅰ中加入一定量的乙醇及研细的溴化钠。充分振荡,混合均匀,并加入沸石(或碎瓷片)。
③将仪器Ⅰ置于石棉网上用小火加热,直至反应结束。此时仪器Ⅱ中已有一定量的液体。
④继续加热直至仪器Ⅰ中的油状液体消失。
⑤将所得到的粗产品依次用水、饱和碳酸氢钠溶液洗涤,最后再用蒸馏水洗涤。
⑥用无水氯化钙干燥后进行蒸馏,得纯溴乙烷。
(1)仪器Ⅰ起两个作用,除了作反应容器,还充当了_____________(仪器)的作用。
(2)步骤②中要在室温下并且在浓H2SO4稀释后才加入溴化钠的原因是:________________。
(3)步骤③中,为什么只能用小火加热,试写出两种不同类型的原因:①________________,②_______________________________________。
(4)步骤⑤中粗产品用水洗涤后,发现有机层仍呈红棕色,为了除去该杂质,可加入饱和亚硫酸氢钠,反应后有二氧化硫生成。试写出该反应的化学方程式:
___________________________________________________________。
(5)装置Ⅰ中的长导管的作用是_____________________________;装置Ⅱ中加入冰的作用是__________________________________________。
(11分)实验室制备气体时,可根据反应物的状态、反应条件和生成气体的性质来选择气体的发生装置。
(1)实验室用氯酸钾和二氧化锰制氧气时,可选用的发生装置是 (写编号);
(2)实验室用食盐固体和浓硫酸制氯化氢气体时,可选用的发生装置是 (写编号),写出微热时的反应方程式 ;
(3)高锰酸钾和二氧化锰都是强氧化剂,均可将浓盐酸氧化为氯气。
(a) 用浓盐酸和高锰酸钾制氯气的反应方程式如下:
2KMnO4 + 16HCl 2KCl + 2MnCl2 +5Cl2
+ 8H2O
①用“单线桥”在上述方程式上标出电子转移的方向和数目。
②反应中 元素被氧化, 是氧化剂。当有1mol电子转移时,可生成气体 升(标准状态下)。
(b) 用浓盐酸和二氧化锰制氯气的实验装置如图所示:
①写出圆底烧瓶中发生反应的化学方程式_
②实验结束清洗仪器时,为了减少烧瓶中残留氯气对环境的污染,可以向烧瓶中加入的溶液是________,有关的化学方程式_________________________.
实验室制备气体时,可根据反应物的状态、反应条件和生成气体的性质来选择气体的发生装置。
| 编号 | A | B | C |
| 发 生 装 置 | 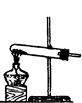 | 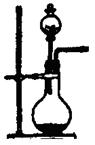 | 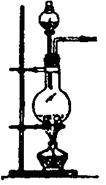 |
 2KCl + 2MnCl2 + 5Cl2 ↑ + 8H2O
2KCl + 2MnCl2 + 5Cl2 ↑ + 8H2O
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com