
题目列表(包括答案和解析)
如何除去下列物质中的少量杂质?并用化学方程式表示.
(1)硫酸亚铁溶液中混有少量硫酸铜.________
(2)铜粉中混有少量铁粉.________
(3)铁粉中混有少量的氧化铁.________
(4)一氧化碳气体中混有少量二氧化碳.________
(5)二氧化碳气体中混有少量一氧化碳.________
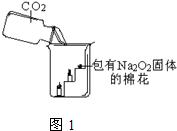 30、过氧化钠(Na2O2)是一种淡黄色固体.在一次科技活动中,某化学兴趣小组的同学将包有Na2O2固体的棉花放入了如图1的实验中,发现了高低不同的两根蜡烛,下面的蜡烛先熄灭,上面的蜡烛后熄灭;同时也惊奇地发现棉花燃烧了起来.
30、过氧化钠(Na2O2)是一种淡黄色固体.在一次科技活动中,某化学兴趣小组的同学将包有Na2O2固体的棉花放入了如图1的实验中,发现了高低不同的两根蜡烛,下面的蜡烛先熄灭,上面的蜡烛后熄灭;同时也惊奇地发现棉花燃烧了起来.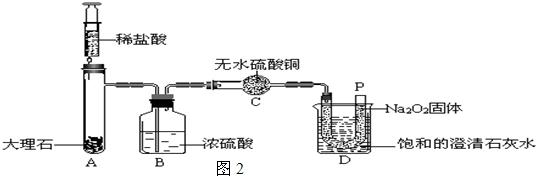

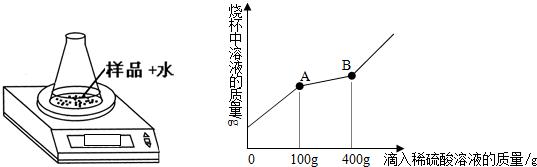
碱式碳酸铜又称“铜绿”也称“铜锈”,是一种绿色粉末.它是由铜在
潮湿的空气中与水、氧气和二氧化碳等物质发生复杂的化学反应生成的.它不溶于水,但却能和盐酸反应,取少量“铜绿”加入试管中,试管中加入少量的稀盐酸,会看到有大量无色气泡冒出,绿色粉末逐渐溶解,将产生的气体通入澄清石灰水,石灰水变混浊.不仅如此,它还能在加热的条件下分解为黑色的氧化铜、水和二氧化碳气体.请回答:
(1)
上述描述碱式碳酸铜的物理性质的语句是:____________________;它的化学性质有①______________________;②__________________.(2)
根据“铜锈”产生的原因以及上面文字的有关内容,请你考虑一下,如果铜生锈了,应该如何除去“铜锈”?你都能想到几种方法?简单叙述一下有关操作.碱式碳酸铜又称“铜绿”也称“铜锈”,是一种绿色粉末.它是由铜在
潮湿的空气中与水、氧气和二氧化碳等物质发生复杂的化学反应生成的.它不溶于水,但却能和盐酸反应,取少量“铜绿”加入试管中,试管中加入少量的稀盐酸,会看到有大量无色气泡冒出,绿色粉末逐渐溶解,将产生的气体通入澄清石灰水,石灰水变混浊.不仅如此,它还能在加热的条件下分解为黑色的氧化铜、水和二氧化碳气体.请回答:
(1)上述描述碱式碳酸铜的物理性质的语句是:____________________;它的化学性质有①______________________;②__________________.
(2)根据“铜锈”产生的原因以及上面文字的有关内容,请你考虑一下,如果铜生锈了,应该如何除去“铜锈”?你都能想到几种方法?简单叙述一下有关操作.
| ||
| △ |
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com